
��T ��ʱ����a g NH3��ȫ����ˮ���õ�V mL��Һ���������Һ���ܶ�Ϊ�� g��cm��3�����ʵ���������Ϊw�����к�NH4+�����ʵ���Ϊb mol��������������ȷ����
A.���ʵ���������Ϊw�� ��100%
��100%
B.���ʵ����ʵ���Ũ��c��1000a/17a mol��L��1
C.��Һ��c(OH��)��1000b/V mol��L��1
D.������Һ���ټ���V mLˮ��������Һ���ʵ�������������0.5w
B
��������
�����������ˮ�������ǰ��������Ը���Һ�����ʵ����ʵ�����a/17mol����Һ�������Vml�������Һ�����ʵ���Ũ����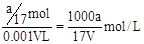 ��ѡ��B��ȷ�����ʵ���������Ϊ
��ѡ��B��ȷ�����ʵ���������Ϊ ��A����ȷ�����ݵ���غ㰱ˮ����c(H+)+c(NH4+)=c(OH-)��c(OH-)>
c(NH4+)=
��A����ȷ�����ݵ���غ㰱ˮ����c(H+)+c(NH4+)=c(OH-)��c(OH-)>
c(NH4+)= ��C����ȷ����ˮ���ܶ�С��ˮ�ģ�����ˮŨ��Խ���ܶ�ԽС�������ٽ���������ˮ��������Һ���ʵ���������С��0.5w��D����ȷ����ѡB��
��C����ȷ����ˮ���ܶ�С��ˮ�ģ�����ˮŨ��Խ���ܶ�ԽС�������ٽ���������ˮ��������Һ���ʵ���������С��0.5w��D����ȷ����ѡB��
���㣺���ʵ���Ũ�ȵļ���
�����������ѶȽϴ��ۺ���ǿ����Ҫ����ѧ��������������������


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
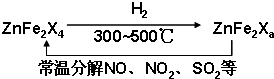
| a |
| Vd-a |
| 1000a |
| 35V |
| 1000b |
| V |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�����ʡ�����ظ���ѧ���������ο��Ի�ѧ�Ծ����������� ���ͣ���ѡ��
��T ��ʱ����a g NH3��ȫ����ˮ���õ�V mL��Һ���������Һ���ܶ�Ϊ�� g��cm��3�����ʵ���������Ϊw�����к�NH4+�����ʵ���Ϊb mol��������������ȷ����
A�����ʵ���������Ϊw�� ��100% ��100% |
| B�����ʵ����ʵ���Ũ��c��1000a/17a mol��L��1 |
| C����Һ��c(OH��)��1000b/V mol��L��1 |
| D��������Һ���ټ���V mLˮ��������Һ���ʵ�������������0.5w |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013������ʡ��У�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��T ��ʱ����a g NH3��ȫ����ˮ���õ�V mL��Һ���������Һ���ܶ�Ϊ�� g/cm3,���ʵ���������Ϊw,���к�NH4+�����ʵ���Ϊb mol��������������ȷ����( )
A�����ʵ���������Ϊw= ��100%
��100%
B�����ʵ����ʵ���Ũ��c= mol/L
mol/L
C����Һ��c(OH-)= mol/L
mol/L
D��������Һ���ټ���V mLˮ��������Һ���ʵ�������������0.5w
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com