
ЁОЬтФПЁПЮЊСЫМьбщЕэЗлЫЎНтЕФВњЮяЃЌЩшМЦШчЯТЪЕбщЗНАИЃК
![]()
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЪдМС1ЮЊ20%ЕФH2SO4ШмвКЃЌЦфзїгУЪЧ_________ЃЛ
ЃЈ2ЃЉЪдМС2ЮЊ_________ЃЌЦфзїгУЪЧ_________ЃЌЪЙМьбщЫЎНтВњЮяЕФЪЕбщЕУвдЫГРћНјааЃЛЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊЃК_________ЃЛ
ЃЈ3ЃЉЗДгІЂйЕФЛЏбЇЗНГЬЪНЮЊ_________ЃЛ
ЃЈ4ЃЉЮЊМьбщЕэЗлвКЪЧЗёвбЭъШЋЫЎНтЃЌШЁЩйСПЫЎНтвКгкЪдЙмжаЃЌМгШыЕтЫЎЃЌдђжЄУїЕэЗлЮДЭъШЋЫЎНтЕФЯжЯѓЪЧ_________ЃЛ
ЃЈ5ЃЉШчЙћЪЕбщЙ§ГЬжаУЛгаМгШыЪдМС2ЖјжБНгМгШыЪдМС3ЃЌФмЗёЪЕЯжЪЕбщФПЕФ_________ЃЈЬюЁБФмЁБЛђЁБЗёЁБЃЉЗёЃЌШєВЛФмЃЌЦфдвђЪЧ_________СђЫсФмШмНтCuЃЈOHЃЉ2ЖјЪЙЪЕбщЪЇАмЃЌзюМђЕЅЕФИФе§ДыЪЉЪЧ_________ЁЃ
ЁОД№АИЁПзїДпЛЏМС ЧтбѕЛЏФЦШмвК жаКЭзїДпЛЏМСЕФСђЫс H++OHЉ=H2O ЃЈC6H10O5ЃЉn+nH2O![]() nC6H12O6 ЕэЗлЦЯЬбЬЧЯдРЖЩЋ Зё СђЫсФмШмНтCuЃЈOHЃЉ2ЖјЪЙЪЕбщЪЇАм жБНгЯђШмвКжаМгШыЩдЙ§СПЕФNaOHШмвК
nC6H12O6 ЕэЗлЦЯЬбЬЧЯдРЖЩЋ Зё СђЫсФмШмНтCuЃЈOHЃЉ2ЖјЪЙЪЕбщЪЇАм жБНгЯђШмвКжаМгШыЩдЙ§СПЕФNaOHШмвК
ЁОНтЮіЁП
(1)ЯЁСђЫсдкЕэЗлЕФЫЎНтЙ§ГЬжазїДпЛЏМСЃЌМгПьСЫЕэЗлЕФЫЎНтЫйТЪЃЛ
(2)ИљОнЧтбѕЛЏЭгыШЉЕФЗДгІашвЊдкМюадЬѕМўЯТЗДгІНјааНтД№ЃЛИљОнжаКЭЗДгІЕФЪЕжЪаДГіЗДгІЕФРызгЗНГЬЪНЃЛ
(3)ЗДгІЂйЮЊЕэЗлЕФЫЎНтЗДгІЃЌЗДгІЩњГЩЦЯЬбЬЧЃЌОнДЫаДГіЗДгІЕФЛЏбЇЗНГЬЪНЃЛ
(4)ШчЙћМгШыЕэЗлКѓЯдЪОРЖЩЋЃЌдђжЄУїЕэЗлУЛгаЭъШЋЫЎНтЃЛ
(5)ИљОнЧтбѕЛЏЭФмЙЛгыЯЁСђЫсЗДгІЕМжТЪЕбщЪЇАмНјааЗжЮіЃЛПЩвдЯђШмвКжаМгШыЧтбѕЛЏФЦШмвКжаКЭЪЃгрЕФСђЫсЁЃ
(1).ЕэЗлЕФЫЎНтЙ§ГЬЃЌБиаыМгШыЯЁСђЫсзїДпЛЏМСЃЌМгПьЕэЗлЕФЫЎНтЗДгІЫйТЪЃЌЙЪД№АИЮЊЃКзїДпЛЏМСЃЛ
(2).ЯЁСђЫсФмЙЛгыЧтбѕЛЏЭЗДгІЃЌЛсЕМжТЪЕбщЪЇАмЃЌЫљвдгІИУЯШМгШыЧтбѕЛЏФЦШмвКжаКЭЯЁСђЫсЃЌЗДгІЕФРызгЗНГЬЪНЮЊЃКH++OH-=H2OЃЌЙЪД№АИЮЊЃКЧтбѕЛЏФЦШмвКЃЛжаКЭзїДпЛЏМСЕФСђЫсЃЛH++OH-=H2OЃЛ
(3).ЕэЗлдкЯЁСђЫсзїгУЯТЭъШЋЫЎНтЩњГЩЦЯЬбЬЧЃЌЫЎНтЗНГЬЪНЮЊЃЈC6H10O5ЃЉn+nH2O![]() nC6H12O6ЃЌЙЪД№АИЮЊЃКЃЈC6H10O5ЃЉn+nH2O
nC6H12O6ЃЌЙЪД№АИЮЊЃКЃЈC6H10O5ЃЉn+nH2O![]() nC6H12O6ЃЛ
nC6H12O6ЃЛ
(4).ЕэЗлгіЕтЯдЪОРЖЩЋЃЌОнДЫПЩвдМьбщЕэЗлЪЧЗёЭъШЋЫЎНтЃЌЗНЗЈЮЊЃКШЁЩйСПЫЎНтвКгкЪдЙмжаЃЌМгШыЕтЫЎЃЌШчЙћШмвКЯдРЖЩЋЃЌдђжЄУїЕэЗлЮДЭъШЋЫЎНтЃЌЙЪД№АИЮЊЃКЯдРЖЩЋЃЛ
(5).ШчЙћВЛМгШыЧтбѕЛЏФЦжаКЭДпЛЏМСЯЁСђЫсЃЌгЩгкСђЫсФмШмНтCu (OH) 2ЖјЪЙЪЕбщЪЇАмЃЌЮоЗЈДяЕНЪЕбщФПЕФЃЛЮЊСЫБмУтЪЕбщЪЇАмЃЌгІИУжБНгЯђШмвКжаМгШыЩдЙ§СПЕФNaOHШмвКжаКЭЯЁСђЫсЃЌЙЪД№АИЮЊЃКЗёЃЛСђЫсФмШмНтCu (OH) 2ЖјЪЙЪЕбщЪЇАмЃЛжБНгЯђШмвКжаМгШыЩдЙ§СПЕФNaOHШмвКЁЃ


 ЛЦИдЙкОќПЮПЮСЗЯЕСаД№АИ
ЛЦИдЙкОќПЮПЮСЗЯЕСаД№АИ ГЄНзївЕБОЭЌВНСЗЯАВсЯЕСаД№АИ
ГЄНзївЕБОЭЌВНСЗЯАВсЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪвЮТЯТЃЌЗДгІHCO3-+H2O![]() H2CO3+OH-ЕФЦНКтГЃЪ§ЮЊ10-8 ЁЃНЋNH4HCO3ШмвККЭАБЫЎАДвЛЖЈБШР§ЛьКЯЃЌПЩгУгкНўШЁЗЯдќжаЕФZnOЁЃШєШмвКЛьКЯв§Ц№ЕФЬхЛ§БфЛЏПЩКіТдЃЌЪвЮТЪБЯТСажИЖЈШмвКжаЮЂСЃЮяжЪЕФСПХЈЖШЙиЯЕе§ШЗЕФЪЧ
H2CO3+OH-ЕФЦНКтГЃЪ§ЮЊ10-8 ЁЃНЋNH4HCO3ШмвККЭАБЫЎАДвЛЖЈБШР§ЛьКЯЃЌПЩгУгкНўШЁЗЯдќжаЕФZnOЁЃШєШмвКЛьКЯв§Ц№ЕФЬхЛ§БфЛЏПЩКіТдЃЌЪвЮТЪБЯТСажИЖЈШмвКжаЮЂСЃЮяжЪЕФСПХЈЖШЙиЯЕе§ШЗЕФЪЧ
A.0.2mol/L АБЫЎЃКc(NH3H2O)>c(NH4+)>c(OH-)>c(H+)
B.0.6 mol/LАБЫЎКЭ0.2 mol/L![]() ШмвКЕШЬхЛ§ЛьКЯЃКc(NH3H2O)+c(CO32-)+c(OH-)=0.3mol/L+2c(H2CO3)+c(H+)
ШмвКЕШЬхЛ§ЛьКЯЃКc(NH3H2O)+c(CO32-)+c(OH-)=0.3mol/L+2c(H2CO3)+c(H+)
C.0.2 mol/LАБЫЎКЭ0.2 mol/L![]() вКЕШЬхЛ§ЛьКЯЃКc(NH4+)+c(NH3H2O)=c(H2CO3)+c(HCO3-)+c(CO32-)
вКЕШЬхЛ§ЛьКЯЃКc(NH4+)+c(NH3H2O)=c(H2CO3)+c(HCO3-)+c(CO32-)
D.0.2mol/L NH4HCO3ШмвК(pH>7)ЃКc(NH4+)>c(HCO3-)>c(H2CO3)>c(NH3H2O)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПввЫсКЭМзЫсМзѕЅЛЅЮЊЭЌЗжвьЙЙЬхЃЌЦфНсЙЙЪНЗжБ№ШчЯТ
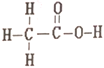 КЭ
КЭ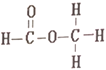
дкЯТСаФФжжМьВтвЧЩЯЯдЪОГіЕФаХКХЪЧЭъШЋЯрЭЌЕФ
A. РюБШЯЃдЊЫиЗжЮівЧ B. КьЭтЙтЦзвЧ
C. КЫДХЙВеёвЧ D. жЪЦзвЧ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊКЭЬМдЊЫиЭЌжїзхЕФXдЊЫиЮЛгкдЊЫижмЦкБэжаЕФЕквЛИіГЄжмЦкЃЌЖЬжмЦкдЊЫиYдзгЕФзюЭтВуЕчзгЪ§БШФкВуЕчзгзмЪ§Щй3ЃЌЫќУЧаЮГЩЛЏКЯЮяЕФЗжзгЪНЪЧXY4ЁЃЪдЛиД№ЃК
(1)XдЊЫиЕФдзгЛљЬЌЪБЕчзгХХВМЪНЮЊЃК___________________________________ЃЌYдЊЫидзгзюЭтВуЕчзгЕФЕчзгХХВМЭМЮЊЃК____________ЁЃ
(2)ШєXЁЂYСНдЊЫиЕчИКадЗжБ№ЮЊ2.1КЭ2.85ЃЌЪдХаЖЯXY4жаXгыYжЎМфЕФЛЏбЇМќЮЊ________(ЬюЁАЙВМлМќЁБЛђЁАРызгМќЁБ)ЁЃ
(3)ИУЛЏКЯЮяЕФПеМфНсЙЙЮЊ______________аЮЃЌжааФдзгЕФЙьЕРдгЛЏРраЭЮЊ__________ЃЌЗжзгЮЊ______________(ЬюЁАМЋадЗжзгЁБЛђЁАЗЧМЋадЗжзгЁБ)ЁЃ
(4)ИУЛЏКЯЮядкГЃЮТЯТЮЊвКЬхЃЌИУвКЬхЮЂСЃМфЕФзїгУСІЪЧ____________ЁЃ
(5)ИУЛЏКЯЮяЕФЗаЕугыSiCl4БШНЯЃК________(ЬюЛЏбЇЪН)ЕФИпЃЌдвђЪЧ_________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖўМзУб(CH3OCH3)ЪЧЮоЩЋЦјЬхЃЌПЩзїЮЊвЛжжаТаЭФмдДЁЃгЩКЯГЩЦј(зщГЩЮЊH2ЁЂCOКЭЩйСПCO2) жБНгжЦБИЖўМзУбЃЌЦфжаЕФжївЊЙ§ГЬАќРЈвдЯТЫФИіЗДгІЃК
ЂйCO(g)+2H2(g)![]() CH3OH(g) ІЄH1=Ѓ90.1kJЁЄmol-1
CH3OH(g) ІЄH1=Ѓ90.1kJЁЄmol-1
ЂкCO2(g)+3H2(g)![]() CH3OH(g)ЃЋH2O(g) ІЄH2=Ѓ49.0kJЁЄmol-1
CH3OH(g)ЃЋH2O(g) ІЄH2=Ѓ49.0kJЁЄmol-1
ЂлCO2(g)ЃЋH2(g) ![]() CO(g)ЃЋH2O(g) ІЄH3=+41.1kJЁЄmol-1
CO(g)ЃЋH2O(g) ІЄH3=+41.1kJЁЄmol-1
Ђм2CH3OH(g)![]() CH3OCH3(g)ЃЋH2O(g) ІЄH4=Ѓ24.5kJЁЄmol-1ЁЃЪдЛиД№ЯТСаЮЪЬтЃК
CH3OCH3(g)ЃЋH2O(g) ІЄH4=Ѓ24.5kJЁЄmol-1ЁЃЪдЛиД№ЯТСаЮЪЬтЃК
(1)гЩH2КЭCOжБНгжЦБИЖўМзУбЕФШШЛЏбЇЗНГЬЪНЃК2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) ІЄH =_______kJЁЄmolЃ1ЃЛИУЗДгІПЩвдздЗЂНјааЕФЬѕМўЮЊ________________ЁЃ
CH3OCH3(g)+H2O(g) ІЄH =_______kJЁЄmolЃ1ЃЛИУЗДгІПЩвдздЗЂНјааЕФЬѕМўЮЊ________________ЁЃ
(2)НЋ1.0mol CO2 КЭ 3.0mol H2 ГфШы2LКуШнУмБеШнЦїжаЃЌЪЙЦфНіАДЗДгІЂкНјааЃЌдкВЛЭЌДпЛЏМСзїгУЯТЃЌЯрЭЌЪБМфФк CO2 ЕФзЊЛЏТЪЫцЮТЖШБфЛЏШчЭМЫљЪОЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ______________
AЃЎT3ЖдгІЕФЦНКтГЃЪ§аЁгкT4ЖдгІЕФЦНКтГЃЪ§
BЃЎИљОнЭМжаЧњЯпЗжЮіЃЌДпЛЏМСIЕФДпЛЏаЇЙћзюКУ
CЃЎbЕуv(е§)ПЩФмЕШгкv(Фц)
DЃЎaЕуЕФзЊЛЏТЪБШcЕуИпПЩФмЕФдвђЪЧИУЗДгІЮЊЗХШШЗДгІЃЌЩ§ЮТЦНКтФцЯђвЦЖЏЃЌзЊЛЏТЪНЕЕЭ
(3)ШєCO2КЭH2НіЗЂЩњЗДгІЂкКЭЂлЃЌбаОПБэУїЃКдкЦфЫћЬѕМўЯрЭЌЕФЧщПіЯТЃЌгУаТаЭДпЛЏМСПЩвдЯджјЬсИпМзДМЕФбЁдёадЃЌЪЙгУИУДпЛЏМСЃЌАД n(CO2)ЃКn(H2)=1ЃК3(змСПЮЊa mol)ЭЖСЯгкКуШнУмБеШнЦїжаНјааЗДгІЃЌCO2ЕФЦНКтзЊЛЏТЪКЭМзДМЕФбЁдёТЪ(МзДМЕФбЁдёТЪЃКзЊЛЏЕФ CO2жаЩњГЩМзДМЕФЮяжЪЕФСПЗжЪ§)ЫцЮТЖШЕФБфЛЏЧїЪЦШчЭМЫљЪОЃКЃЈКіТдЮТЖШЖдДпЛЏМСЕФгАЯьЃЉ
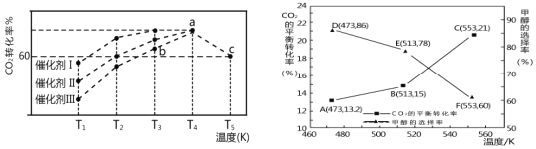
Ђйдк553KДяЕНЦНКтЪБЃЌЗДгІЬхЯЕФкМзДМЕФЮяжЪЕФСПЮЊ_________molЁЃ
ЂкЫцзХЮТЖШЕФЩ§ИпЃЌCO2ЕФЦНКтзЊЛЏТЪдіМгЕЋМзДМЕФбЁдёТЪНЕЕЭЃЌЧыЗжЮіЦфдвђЃК____________________________ ЁЃ
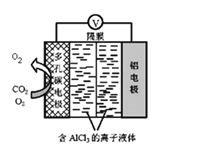
(4)O2ДпЛЏИЈжњЕФ Al-CO2ЕчГиЙЄзїдРэШчЭМЫљЪОЁЃИУЕчГиЕчШнСПДѓЃЌФмгааЇРћгУCO2ЃЌЕчГиЗДгІВњЮяAl2(C2O4)3ЪЧживЊЕФЛЏЙЄдСЯЁЃ дђЕчГиЕФе§МЋЗДгІЪНЃК6O2+6e-=6O2-КЭ____________________ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЃКЂй![]() ЃЋHNO3
ЃЋHNO3![]() ЃЋH2O ІЄHЃМ0ЃЛЂкЯѕЛљБНЗаЕу210.9ЁцЃЌеєСѓЪБбЁгУПеЦјРфФ§ЙмЁЃЯТСажЦШЁЯѕЛљБНЕФВйзїЛђзАжУЃЈВПЗжМаГжвЧЦїТдШЅЃЉЃЌе§ШЗЕФЪЧ
ЃЋH2O ІЄHЃМ0ЃЛЂкЯѕЛљБНЗаЕу210.9ЁцЃЌеєСѓЪБбЁгУПеЦјРфФ§ЙмЁЃЯТСажЦШЁЯѕЛљБНЕФВйзїЛђзАжУЃЈВПЗжМаГжвЧЦїТдШЅЃЉЃЌе§ШЗЕФЪЧ
A.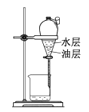 ЗжвКB.
ЗжвКB.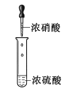 ХфжЦЛьЫс
ХфжЦЛьЫс
C.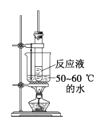 ЫЎдЁМгШШD.
ЫЎдЁМгШШD.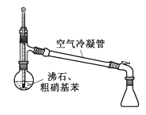 еєСѓЬсДП
еєСѓЬсДП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪвКЯГЩввЫсввѕЅЕФВНжшШчЯТЃКдкЭММзЕФдВЕзЩеЦПФкМгШыввДМЁЂХЈСђЫсКЭввЫсЃЌМгШШЛиСївЛЖЮЪБМфЃЌШЛКѓЛЛГЩЭМввзАжУНјааеєСѓЃЌЕУЕНКЌгаввДМЁЂввЫсКЭЫЎЕФввЫсввѕЅДжВњЦЗЁЃ
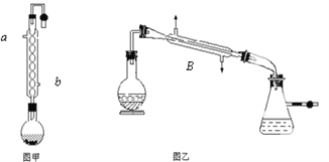
ЧыЛиД№ЯТСаЮЪЬт
ЃЈ1ЃЉЭММзжаРфФ§ЫЎДг______ЃЈaЛђbЃЉНјЃЌЭМввжаBзАжУЕФУћГЦЮЊ_______ЃЛ
ЃЈ2ЃЉЭММздкЩеЦПжаГ§СЫМгШыввДМЁЂХЈСђЫсКЭввЫсЭтЃЌЛЙгІЗХШыЗаЪЏЃЌФПЕФЪЧ_______ЃЛ
ЃЈ3ЃЉЗДгІжаМгШыЙ§СПЕФввДМЃЌФПЕФЪЧ_______ЃЛ
ЃЈ4ЃЉЯжФтЗжРыДжВњЦЗввЫсввѕЅЁЂввЫсКЭввДМЕФЛьКЯЮяЯТСаПђЭМЪЧЗжРыВйзїВНжшСїГЬЭМЃК
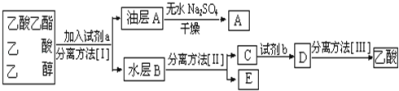
дђЪдМСaЪЧ______ЃЌЗжРыЗНЗЈIЪЧ_______ЃЌЗжРыЗНЗЈIIЪЧ_______ЃЌВњЮяEЪЧ______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУЯЕЭГУќУћЗЈУќУћЛђаДГіНсЙЙМђЪНЃК
ЃЈ1ЃЉ3-МзЛљ-2-БћЛљ-1-ЮьЯЉЕФНсЙЙМђЪНЮЊ______________________________
ЃЈ2ЃЉ![]() УћГЦЮЊ_______________________________________
УћГЦЮЊ_______________________________________
ЃЈ3ЃЉ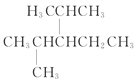 УћГЦЮЊЃК________________________________
УћГЦЮЊЃК________________________________
ЃЈ4ЃЉ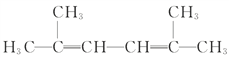 УћГЦЮЊЃК_______________
УћГЦЮЊЃК_______________
ЃЈ5ЃЉ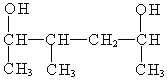 УћГЦЮЊЃК___________________________
УћГЦЮЊЃК___________________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙигк![]() ЕФа№ЪіДэЮѓЕФЪЧ( )
ЕФа№ЪіДэЮѓЕФЪЧ( )
A.ЪЧСНадЧтбѕЛЏЮя
B.ЪЧФбШмгкЫЎЕФАзЩЋНКзДЮяжЪЃЌЪЧШѕЕчНтжЪ
C.МШШмгкАБЫЎЃЌгжФмШмгкДзЫс
D.ФмФ§ОлЫЎжааќИЁЮяЃЌПЩгУзіОЛЫЎМС
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com