
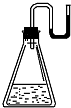
 有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④金属钠.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如图所示状态,判断加入的物质可能是( )
有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④金属钠.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如图所示状态,判断加入的物质可能是( )| A. | ①②③④ | B. | ①②④ | C. | ②③④ | D. | ①②③ |
分析 由图可知,发现U形管内的滴有红墨水的水面左低右高,则物质与水反应生成气体或反应放热,以此来解答.
解答 解:由图可知,发现U形管内的滴有红墨水的水面左低右高,则物质与水反应生成气体或反应放热,
①NaOH固体溶于水,放热,锥形瓶中气体压强增大,U形管内的滴有红墨水的水面左低右高,故选;
②浓硫酸与水混合放热,锥形瓶中气体压强增大,U形管内的滴有红墨水的水面左低右高,故选;
③NH4NO3晶体与水混合,吸热,U形管内的滴有红墨水的水面左高右低,故不选;
④金属钠与水反应生成氢气,锥形瓶中气体压强增大,U形管内的滴有红墨水的水面左低右高,故选;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:选择题
 科学家研制出多种新型杀虫剂代替DDT,化合物A是其中的一种,其结构如图.下列关于A的说法正确的是( )
科学家研制出多种新型杀虫剂代替DDT,化合物A是其中的一种,其结构如图.下列关于A的说法正确的是( )| A. | 化合物A的分子式为C15H22O3 | |
| B. | 与FeCl3溶液发生反应后溶液显紫色 | |
| C. | 1 mol A最多可以与2 mol Cu(OH)2反应 | |
| D. | 1 mol A最多与1 mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 磷是生物体中不可缺少的元素之一,它能形成多种化合物.
磷是生物体中不可缺少的元素之一,它能形成多种化合物.查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 ;C 的结构简式:CH3CHO
;C 的结构简式:CH3CHO查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com