
(8分每空1分)
(1)下列3种不同粒子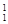 H、
H、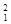 H、
H、 H表示______种元素,______种核素,
H表示______种元素,______种核素,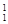 H、
H、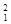 H、
H、 H互称为__________________。
H互称为__________________。
(2)下列各组物质中,互称为同分异构体的是( )
| A.水与冰 | B.O2与O3 |
C.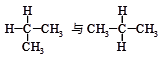 | D. |
科目:高中化学 来源: 题型:单选题
1898年,IUPAC(International Union of Pure and Applied Chemistry,国际纯粹与应用化学联合会)建议用1~18列代替原周期表中主族、副族序号,请问原第IVA族应该在第几列?
| A.第4列 | B.第14列 |
| C.第5列 | D.第15列 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。
| A | | C |
| | B | |
 反应的化学方
反应的化学方 查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(第1小题1分,其余每空2分,共11 分)
短周期元素A、B、C、D中,0.5 mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4 g A的氧化物恰好与100 mL 0.2 mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素是第二周期中原子半径最小的元素,C2-比A元素的离子多1个电子层,D元素的原子核外L层比K层多2个电子。
(1)B元素的名称是 。
(2)画出D和C2-的结构示意图 。______________________。
(3)将B元素形成的单质通入水中反应的化学方程式为_________________________, B、C、D三种元素形成的氢化物中稳定性最强的是_______(填写化学式,下同),最高价氧化物的水化物酸性最强的是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(11分)原子序数依次增大的短周期元素A、B、C、D、E、F,其中 A、B的阴离子与C、D的阳离子的电子排布式均为ls22s22p6,A原子核外有2个未成对电子,C单质可与热水反应但不能与冷水反应;E、F原子在基态时填充电子的轨道有9个,且E原子核外有3个未成对电子,F能形成与A相同价态的阴离子,且A离子半径小于F离子。回答:
(1)B元素的名称为 。
(2)A与F可形成两种中学化学常见的化合物,其分子式分别为 和 ;分子空间构型分别为 。
(3)请写出基态原子E的价电子排布式
(4)上述六种元素按电负性从大到小的排列是 (写元素符号表示)。
(5)C、D、E、F元素第一电离能从小到大的排列是 (写元素符号);
(6)A、B、C、D四种元素的简单离子按半径由小到大的顺序为(用离子符号表示)__________________________。
(7)C与A形成的化合物属于 晶体,此化合物和NaCl固体相比较熔点的高低关系为
(用化学式表示大小关系),原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | | | | ① | ② | ③ | | |
| 3 | ④ | | ⑤ | | | ⑥ | ⑦ | ⑧ |
| 4 | ⑨ | | | | | | | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(8分)元素A、B、C都是短周期元素,A元素原子的2p轨道上只有两个未成对电子,B的3p轨道上有空轨道,A、B同主族,B、C同周期,C是本周期中电负性最大的。请回答:
(1)A原子的核外电子排布的轨道表示式________,B原子的核外电子排布式__________________,C原子的价电子排布式________。
(2)A、B、C的气态氢化物中最不稳定的是________(填化学式)。
(3) A、B、C的最高价氧化物的水化物中,酸性最强的是________。
(4)AC4的结构式为________,中心原子A的杂化方式________杂化,是________(填“极性”或“非极性”)分子。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分).
Ⅰ. 下表列出了A~R 9种元素在周期表中的位置(填元素符号):
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | E | | F | | |
| 3 | A | C | D | | | | G | R |
| 4 | B | | | | | | H | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com