
醋酸溶液中存在电离平衡:CH3COOH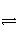
 H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )
A.CH3COOH溶液中离子浓度的关系满足:[H+]=[OH-]+[CH3COO-]
B.0.1 mol·L-1的CH3COOH溶液加水稀释,溶液中[OH-]增大
C.CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动
D.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
科目:高中化学 来源: 题型:
若pH=3的酸溶液和pH=11的碱溶液等体积混合后 溶液呈酸性,其原因可能是
A.生成了一种强酸弱碱盐 B.弱酸溶液和强碱溶液反应
C.强酸溶液和弱碱溶液反应 D.一元强酸溶液和一元强碱溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2 mol·L-1的盐酸与等体积水混合后pH=1
D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
|
| A. | 碳酸氢钠的水解:HCO3﹣+H2O⇌H3O++CO32﹣ |
|
| B. | 以硫酸铝和小苏打为主要反应物的泡沫灭火器中的反应原理:Al3++3HCO3﹣═Al(OH)3↓+3CO2↑ |
|
| C. | 1 mol/L NH4Al(SO4)2溶液中逐滴加入等体积4 mol/L NaOH溶液:Al3++4OH﹣═AlO2﹣+2H2O |
|
| D. | 用惰性电极电解AlCl3溶液:2Cl﹣+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
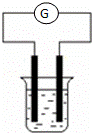
现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下:
| G 实验分组 | 所用金属 | 电子流向 |
| ① | A、Cu | A→Cu |
| ② | C、D | D→C |
| ③ | A、C | C→A |
| ④ | B、Cu | Cu→B |
| ⑤ | … | … |
根据上述情况,回答下列问题:
(1)上述五种金属的活动性顺序是 .
(2)在①中,Cu片上观察到的现象是: ;
(3)在②中,溶液中H+向金属片 移动;
(4)在④中,两金属片上均无气泡放出.此时两金属片上的电极反应式分别为:Cu: ;B: ;
(5)如果实验⑤用B、D,则导线中电流方向为: (填B→D或D→B);
(6)已知反应:Cu+2Fe3+═Cu2++2Fe2+.请用下列试剂和材料,用上图所示装置,将此反应设计成原电池并检验正极产物.
试剂:CuCl2溶液、FeCl3溶液、FeCl2溶液、KSCN溶液、K3[Fe(CN)6]溶液、双氧水、NaOH溶液
材料:Cu片、Fe片、石墨棒
a、设计电池应选用的试剂和材料是: ;
b、检验正极产物选用的试剂是 ,检验反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| 化学式 | 电离常数 |
| HClO | K=3×10-8 mol·L-1 |
| H2CO3 | K1=4.3×10-7 mol·L-1 |
| K2=5.6×10-11 mol·L-1 |
A.[HCO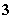 ]>[ClO-]>[OH-]
]>[ClO-]>[OH-]
B.[ClO-]>[HCO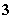 ]>[H+]
]>[H+]
C.[HClO]+[ClO-]=[HCO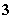 ]+[H2CO3]
]+[H2CO3]
D.[Na+]+[H+]=[HCO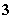 ]+[ClO-]+[OH-]
]+[ClO-]+[OH-]
查看答案和解析>>
科目:高中化学 来源: 题型:
某酸式盐NaHY的水溶液中有[OH-]>[H+],下列叙述正确的是( )
A.H2Y的电离方程式:H2Y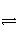
 2H++Y2-
2H++Y2-
B.HY-的水解方程式:HY-+H2O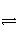
 H3O++Y2-
H3O++Y2-
C.该酸式盐溶液中离子浓度关系:[Na+]>[HY-]>[OH-]>[H+]
D.该酸式盐溶液中离子浓度关系:[Na+]>[Y2-]>[HY-]>[OH-]>[H+]
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如下表,下列叙述正确的是
| 酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数 | K a=1.75×10-5 | K a=2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
A.25℃,等物质的量浓度的CH3COONa、NaClO、Na2CO3和Na2SO3 四种溶液中,碱性最强的是Na2CO3
B.将0.1 mol·L-1的醋酸加水不断稀释,所有离子浓度均减小
C.少量的SO2通入Ca(ClO)2溶液中反应的离子方程式为:
SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
D.少量CO2通入NaClO溶液中反应的离子方程式为:CO2+H2O+2ClO-=CO32-+2HClO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com