
【题目】在下列各组离子中,能大量共存的( )
A.Ag+、NO3﹣、Na+、Cl﹣
B.K+、HCO3﹣、Cl﹣、Al3+
C.NO3﹣、Fe2+、H+、Br﹣
D.K+、Cl﹣、SO42﹣、NH4+
科目:高中化学 来源: 题型:
【题目】下列物质的分离方法不正确的是( )
A.用结晶的方法分离汽油和水
B.用过滤的方法除去氯化钠溶液中的泥沙
C.用重结晶的方法从含有少量氯化钠的硝酸钾溶液中提取硝酸钾
D.蒸馏法分离乙酸(沸点118)和乙酸乙酯(沸点77.1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴及其化合物可应用与催化剂、电池、颜料与染料等。
(1)CoO是一种油漆添加剂,可通过反应①②制备。
①2Co(s)+O2(g)=2CoO(s) ΔH1=akJ·mol-1
②2CoCO3(s) =CoO(s) + CO2 (g) ΔH2=akJ·mol-1
则反应2Co(s)+O2(g)+2CO2(g)=2CoO3(s) 的ΔH=_________。
(2)某锂电池的电解质可传导Li+,电池反应式为:LiC6+CoO2![]() C6+LiCoO2
C6+LiCoO2
①电池放电时,负极的电极反应式为_________,Li+向______移动(填“正极”或“负极“)。
②一种回收电极中Co元素的方法是:将LiCoO2与H2O2、H2SO4反应生成CoSO4。该反应的化学方程式为___________________。
(3)BASF高压法制备醋酸采用钴碘催化循环过程如图-1所示,该循环的总反应方程式为_________________(反应条件无需列出)
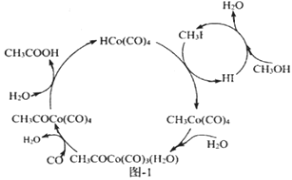
(4)某含钴催化剂可同时催化去除柴油车尾气中的碳烟(C)和NOx。不同温度下,将10mol模拟尾气(成分如下表所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图-2所示.
模拟尾气 | 气体 | 碳烟 | ||
NO | O2 | He | ||
物质的量分数或物质的量 | 0.25% | 5% | 94.75% | a mol |
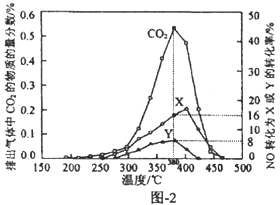
①380℃时,测得排出的气体中含0.45 mol O2和0.0525 mol CO2,则Y的化学式为__________________。
②实验过程中采用NO模拟NOx,,而不采用NO2的原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、硫的含量影响钢铁性能。某兴趣小组用如下流程对钢样进行探究。
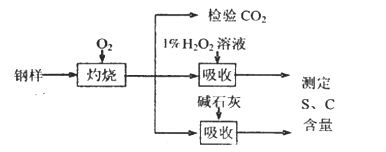
(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为_____________。
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是____________ (填字母)。
a.酸性KMnO4溶液 b.澄清石灰水 c.饱和小苏打溶液 d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000 mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U型管(如下图),碱石灰增重0.614 g。
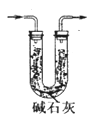
①用l%H2O2溶液吸收SO2,发生反应的离子方程式为___________________。
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是______________(填字母)
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与我们人类生活息息相关,下列说法不正确的是
A. 开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径
B. 工业上,电解熔融MgCl2制金属镁
C. 研发使用高效催化剂,可提高反应中原料的转化率
D. “冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是()
A. 不含其他杂质的天然油脂属于纯净物
B. 肥皂的有效成分为硬脂酸钠和甘油
C. 油脂的烃基部分饱和程度越大,熔点越低
D. 各种油脂水解后的产物中都有甘油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个2 L的密闭容器中反应CO2(g)+H2(g) ![]() CO(g)+H2O(g) 达到平衡,下列说法正确的是
CO(g)+H2O(g) 达到平衡,下列说法正确的是
容器 | 温度/℃ | 初始物质的量/mol | 平衡物质的量/mol | |
n(CO2) | n(H2) | n(CO) | ||
Ⅰ | 700 | 1.50 | 1.00 | 0.6 |
Ⅱ | 700 | 3.00 | 2.00 | |
Ⅲ | 800 | 1.50 | 1.00 | 0.8 |
A.该反应的正反应为放热反应
B.达到平衡时,容器Ⅱ中CO的体积分数比容器Ⅲ中的小
C.达到平衡时,容器Ⅰ和容器Ⅱ反应物的转化率、反应速率均相等
D.容器Ⅱ中反应5分钟达到平衡,则该时间段v(CO)=0.24 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是你,化学是我,化学深入我们的生活。下列说法不正确的是( )
A. 石油经过分馏可以得到汽油,汽油仍然属于混合物
B. 煤的气化与液化都是化学变化
C. 包装用材料聚乙烯、聚丙烯和聚氯乙烯都属于烃
D. 用浸泡过KMnO4溶液的硅藻土保存水果可以消除乙烯的影响使水果保鲜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(化学组成为FeC2O4·2H2O)是一种淡黄色晶体粉末,是生产锂电池的原材料。已知FeC2O4·2H2O在300 ℃左右完全分解生成FeO、CO2、CO、H2O四种氧化物。某学习小组欲验证草酸亚铁晶体的分解产物。
I.甲组同学设计了如下实验装置:

(1)实验开始前,鼓入氮气的目的是____________。
(2)实验中,装置B中的现象是 。
(3)装置C中可观察到的现象是_________,由此可知草酸晶体分解的产物中有_______。
(4)设计实验验证装置A中黑色残留物不含有Fe3O4 (简要说明实验操作,现象和结论)。
II.乙组同学选用甲组实验中的装置A(接口用x表示)和下图所示的装置(可以重复选用)验证分解产物CO。
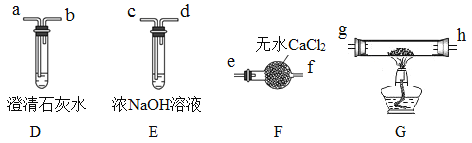
(5)乙组同学的实验装置中,依次连接的合理顺序为x→______g→h→a(用接口字母和“→”表示)。装置G反应管中盛有的物质是_______。能证明草酸晶体分解产物中有CO的现象是_______。
(6)按照题目提供的装置和要求设计的实验明显存在的一个不足是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com