
科目: 来源:不详 题型:单选题
| A.①、② | B.②、④ | C.②、③ | D.③、④ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.0.44s | B.1s | C.1.33s | D.2s |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| c(H2)(mol?L-1) | c(Cl2)(mol?L-1) | υ(mol?L-1?S-1) |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 4.0k |
| A.m=1,n=1 | B.m=
| C.m=
| D.m=1,n=
|
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.20mLmol/LHCl溶液 | B.30mLmol/HCl溶液 |
| C.10mLmol/CH3COOH溶液 | D.10mLmol/LH2SO4溶液 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:问答题

| c(CO2)? c(H2) |
| c(CO)?c(H2O) |
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 时间/s c/mol?L-1 |
0 | 20 | 40 | 60 | 80 | 100 |
| N2O4 | 0.20 | a | 0.10 | c | d | e |
| NO2 | 0 | 0.12 | b | 0.26 | 0.30 | 0.30 |
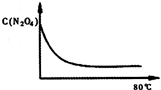
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.v(甲)>v(乙)>v(丙) | B.v(乙)>v(丙)>v(甲) |
| C.v(丙)>v(甲)>v(乙) | D.v(乙)>v(甲)>v(丙) |
查看答案和解析>>
科目: 来源:不详 题型:多选题
| 实验序号 | c(CO)/mol.L-1 | c(Cl2)/mol.L-1 | ν/mol.L-1.s-1 |
| 1 | 0.100 | 0.100 | 1.2×10-2 |
| 2 | 0.100 | 0.050 | 6.0×10-3 |
| 3 | 0.050 | 0.100 | 6.0×10-3 |
| A.m=1n=1 | B.m=2n=1 | C.n=1.5k=0.6 | D.m=1k=1.2 |
查看答案和解析>>
科目: 来源:崇明县二模 题型:问答题

| 时间(S) | 0 | 20 | 40 | 60 | 80 | 100 |
| n( N2O4 )(mol) | 0.80 | a | 0.40 | c | d | e |
| n(NO2)(mol) | 0.00 | 0.48 | b | 1.04 | 1.20 | 1.20 |
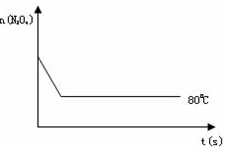
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com