
科目: 来源:不详 题型:问答题
| 催化剂 |
| △ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.将反应温度升高至1200 K |
| B.将压强减小至原来的一半 |
| C.添加催化剂 |
| D.增大水蒸气的浓度 |
查看答案和解析>>
科目: 来源:不详 题型:单选题

| A.0.68 | B.0.34 | C.0.45 | D.0.47 |
查看答案和解析>>
科目: 来源:不详 题型:单选题

| A.降低温度 | B.增大压力 |
| C.加入氧气 | D.去掉三氧化硫 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
A.K=
| ||
B.K=
| ||
C.K=
| ||
D.K=
|
查看答案和解析>>
科目: 来源:不详 题型:填空题
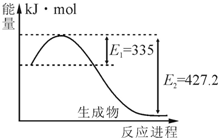
| ||
| (一定条件) |
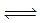
| C(N2)?[C (H2) ]3 |
| [C (NH3)]2 |
| t/K | 298 | 398 | 498 | … |
| K/(mol?L-1)-2 | 4.1×106 | K1 | K2 | … |
查看答案和解析>>
科目: 来源:不详 题型:问答题

| 温度/°C | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |

查看答案和解析>>
科目: 来源:如皋市模拟 题型:问答题
| 活性炭 |
查看答案和解析>>
科目: 来源:西安模拟 题型:问答题
| ||
查看答案和解析>>
科目: 来源:广东 题型:单选题
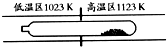
| A.在不同温度区域,TaI4的量保持不变 |
| B.在提纯过程中,I2的量不断减少 |
| C.在提纯过程中,I2的作用是将TaS2从高温区转移到低温区 |
| D.该反应的平衡常数与TaI4和S2的浓度乘积成反比 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com