
科目: 来源:广东模拟 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.2.3×10-7mol?L-1 | B.4.6×10-7mol?L-1 | ||
| C.9.2×10-7mol?L-1 | D.
|
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 难溶电解质 | AgCl | AgBr | AgI | Ag2SO4 | Ag2CrO4 |
| Ksp | 1.8×10-10 | 5.4×10-13 | 8.5×10-17 | 1.4×10-5 | 1.12×10-12 |
| A.Ksp的大小与三种卤化银见光分解的难易无关 |
| B.将等体积的4×10-3mo1?L-1的AgNO3和4×10-3mo1?L-1K2CrO4混合,有Ag2CrO4沉淀产生 |
| C.向AgCl的悬浊液中滴加NaI的饱和溶液可以得到黄色AgI悬浊液 |
| D.100mL0.1mol?L-1的Na2SO4溶液中加入1mL0.1mol?L-1的AgNO3溶液,有白色沉淀生成 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
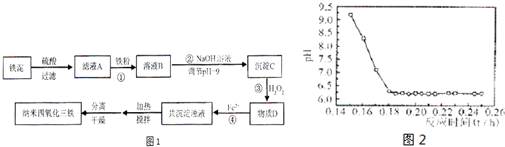
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.NH3?H2O | B.MgO | C.Mg(OH)2 | D.MgCO3 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.根据Ksp(AgCl)=1.77×10-10,Ksp(Ag2CrO4)=1.12×10-12,可以推知AgCl的溶解度比Ag2CrO4的溶解度大 |
| B.0.1mol?L-1的ZnCl2溶液中通入足量硫化氢气体,最终得不到ZnS沉淀.是因为溶液中c(Zn2+)?c(S2-)>Ksp(ZnS) |
| C.向硫酸钡沉淀中加入碳酸钠溶液,沉淀发生转化,据此可推知碳酸钡的Ksp比硫酸钡的小 |
| D.AgCl在10mL 0.05mol?L-1的KCl溶液中比在20mL0.01mol?L-1的AgNO3溶液中溶解的质量少 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
| 实验序号 | FeSO4溶液的体积读数/mL | |
| 滴定前 | 滴定后 | |
| 1 | 0.10 | 16.20 |
| 2 | 0.30 | 15.31 |
| 3 | 0.20 | 15.19 |
查看答案和解析>>
科目: 来源:聊城模拟 题型:问答题
| 1 |
| 2 |
| 10 |
| 3 |
c(C
| ||
c(S
|

查看答案和解析>>
科目: 来源:青岛模拟 题型:单选题
| A.25℃时,0.1mol?L-1HF溶液中pH=1 |
| B.Ksp(CaF2)随温度和浓度的变化而变化 |
| C.加入CaCl2溶液后体系中的c(H+)浓度不变 |
| D.该体系中有CaF2沉淀产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com