
科目: 来源:南昌模拟 题型:问答题
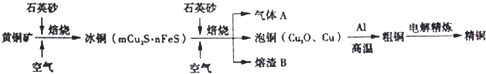
查看答案和解析>>
科目: 来源:重庆 题型:问答题
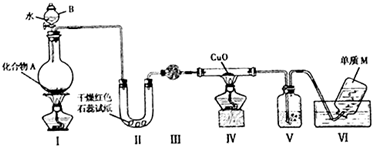
查看答案和解析>>
科目: 来源:深圳模拟 题型:问答题
| 实验操作 | 预期现象和结论 |
| 步骤1:用药匙取少量白色粉末于试管A底部,点燃酒精灯,充分加热试管. | ______ |
| 步骤2:______ | ______ |
| 步骤3:______ | ______ |
| 步骤4:______ | ______ |
| … |
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:通州区一模 题型:填空题
| ① | ② | ③ | |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 硅 胶 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
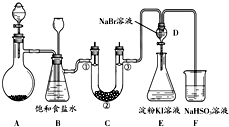
查看答案和解析>>
科目: 来源:不详 题型:问答题

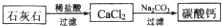
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:问答题

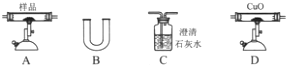
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 阴离子 | SO42-、NO3-、Cl- |
| 阳离子 | Fe3+、Fe2+、NH4+、Cu2+、Al3+ |
查看答案和解析>>
科目: 来源:合肥一模 题型:填空题
| 实验步骤 | 预期现象与结论 |
步骤1:取少量上述溶液注入试管中,滴入几滴淀粉溶液振荡. |
若溶液显______,则假设1成立;否则,假设1不成立,再进行步骤2 |
步骤2:______ ______ ______ |
若溶液显蓝色,则假设2成立,反应的离子方程式为______;否则,假设2不成立,再进行步骤3 |
步骤3:______ ______ ______ |
______ ______ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com