
科目: 来源:同步题 题型:填空题

查看答案和解析>>
科目: 来源:安徽省模拟题 题型:填空题
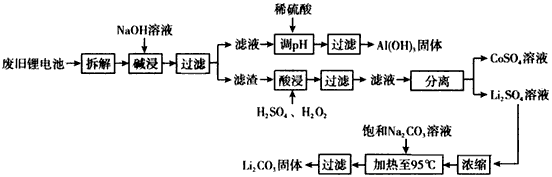
查看答案和解析>>
科目: 来源:同步题 题型:填空题
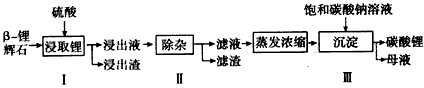
查看答案和解析>>
科目: 来源:江苏模拟题 题型:填空题
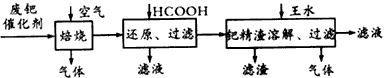
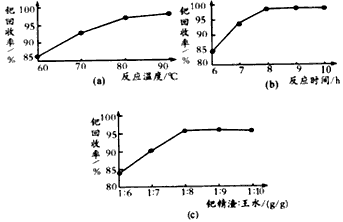
查看答案和解析>>
科目: 来源:同步题 题型:填空题
查看答案和解析>>
科目: 来源:同步题 题型:填空题
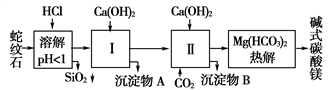
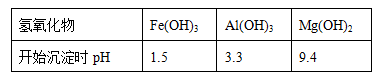
查看答案和解析>>
科目: 来源:广东省高考真题 题型:填空题
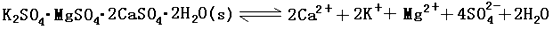
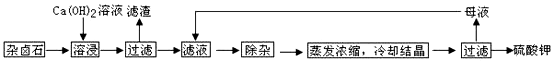
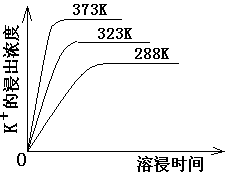
 已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K(计算结果保留三位有效数字)。
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K(计算结果保留三位有效数字)。查看答案和解析>>
科目: 来源:高考真题 题型:填空题

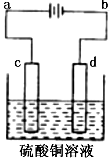
查看答案和解析>>
科目: 来源:江西省模拟题 题型:填空题
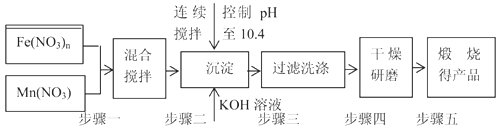
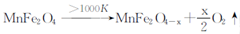 ,
,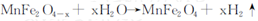
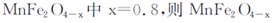 ,中Fe2+占全部铁元素的百分率为__________。
,中Fe2+占全部铁元素的百分率为__________。查看答案和解析>>
科目: 来源:陕西省模拟题 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com