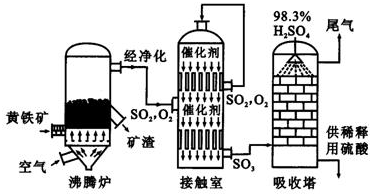
以黄铁矿为原料生产硫酸的工艺流程图如下:
(1)将燃烧黄铁矿的化学方程式补充完整:4
FeS2
FeS2
+11O
22Fe
2O
3+8SO
2(2)接触室中发生反应的化学方程式是
.
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)
abd
abd
.
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO
2的转化率
c.使用催化剂能提高SO
2的反应速率和转化率
d.沸腾炉排出的矿渣可制造水泥或制砖,含铁品位高的矿渣可炼铁
(4)每160g SO
3气体与液态H
2O化合放出260.6kJ的热量,该反应的热化学方程式是
SO3(g)+H2O(l)=H2SO4(l);△H=-130.3kJ/mol
SO3(g)+H2O(l)=H2SO4(l);△H=-130.3kJ/mol
.
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO
2和铵盐.
①SO
2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br
2.SO
2吸收Br
2的离子方程式是
SO2+Br2+2H2O=4H++2Br-+SO42-
SO2+Br2+2H2O=4H++2Br-+SO42-
.
②为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解).该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量.铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变.计算:该铵盐中氮元素的质量分数是
14.56
14.56
%;若铵盐质量为15.00g,浓硫酸增加的质量为
2.31g
2.31g
.(计算结果保留两位小数)

 A、B、C、D、E、W均为短周期元素,原子序数依次增大.回答下列问题:
A、B、C、D、E、W均为短周期元素,原子序数依次增大.回答下列问题: