
科目: 来源: 题型:
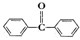 )及其衍生物,第Ⅱ类为苯甲酸苯酯(
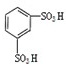
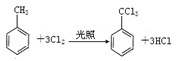
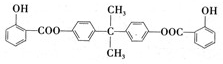
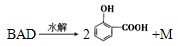
)及其衍生物,第Ⅱ类为苯甲酸苯酯(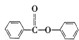 )的衍生物,某紫外线吸收剂UV-0(属于第Ⅰ类产品)的合成路线如下:
)的衍生物,某紫外线吸收剂UV-0(属于第Ⅰ类产品)的合成路线如下: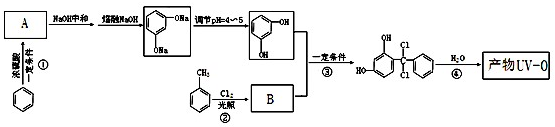
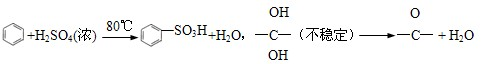


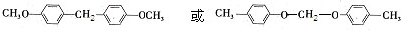
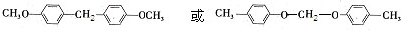
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| 阴离子 | SO42-、NO3-、Cl- |
| 阳离子 | Fe3+、Fe2+、NH4+、Cu2+、Al3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com