
科目: 来源: 题型:选择题
| A. | 实验①能证明K2Cr2O7溶液中存在上述平衡 | |
| B. | 实验②能说明氧化性:Cr2O72->Fe3+ | |
| C. | CrO42-和Fe2+在酸性溶液中可以大量共存 | |
| D. | 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | KClO3=K++Cl-+3O2- | B. | K2CO3=2K++CO32- | ||
| C. | NaOH=Na++OH- | D. | NH4Cl=NH4++Cl- |
查看答案和解析>>
科目: 来源: 题型:填空题
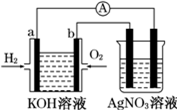 化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.查看答案和解析>>
科目: 来源: 题型:解答题
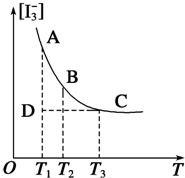 实验室中配制碘水,往往是将I2溶于KI溶液中,这样就可以得到浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq)?I3-(aq).上述平衡体系中,I3-的物质的量浓度[I3-]与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).
实验室中配制碘水,往往是将I2溶于KI溶液中,这样就可以得到浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq)?I3-(aq).上述平衡体系中,I3-的物质的量浓度[I3-]与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).查看答案和解析>>
科目: 来源: 题型:选择题
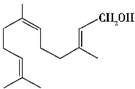
| A. | 金合欢醇与乙醇是同系物 | |
| B. | 金合欢醇可发生加成反应,但不能发生取代反应 | |
| C. | 1 mol 金合欢醇能与3 mol H2 反应,也能与3 mol Br2反应 | |
| D. | 1 mol 金合欢醇与足量Na 反应生成1mol 氢气,完全燃烧时消耗O2 21 mol |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 1mol纯物质完全燃烧时所放出的热量,叫该物质的燃烧热 | |
| B. | 放热反应热化学方程式中△H就是该反应物的燃烧热 | |
| C. | 物质的燃烧热可利用仪器由实验测得 | |
| D. | 物质燃烧必然伴随发光发热现象且肯定是氧化还原反应 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 在任何条件下,化学平衡常数都是一个定值 | |
| B. | 当改变反应物的浓度时,化学平衡常数会发生改变 | |
| C. | 化学平衡常数K只与温度有关,与反应物浓度、体系的压强无关 | |
| D. | 化学平衡常数K可以推断一个可逆反应进行的程度 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{1}{3}$B2H6 (g)+O2 (g)═$\frac{1}{3}$B2O3 (g)+H2O (g)△H=-677.7 kJ•mol-1 | |
| B. | B2H6 (g)+3O2 (g)═B2O3(s)+3H2O (g)△H=-2165 kJ•mol-1 | |
| C. | B2H6 (g)+3O2 (g)═B2O3(s)+3H2O (g)△H=-2033 kJ•mol-1 | |
| D. | B2H6 (g)+3O2 (g)═B2O3(s)+3H2O(l)△H=-2033 kJ•mol-1 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com