
科目: 来源: 题型:
 Ⅰ、写出甲烷燃料电池在酸性溶液中的电极反应和总电池反应:
Ⅰ、写出甲烷燃料电池在酸性溶液中的电极反应和总电池反应:| 周围变红的电极代号(填字母) | 原因 |
A A |
O2+2H2O+4e-=4OH-,产生OH- O2+2H2O+4e-=4OH-,产生OH- |
E E |
2H++2e-=H2↑ H+反应,促进了水的电离,溶液中c(OH-)>c(H+) 2H++2e-=H2↑ H+反应,促进了水的电离,溶液中c(OH-)>c(H+) |
无 无 |
无 无 |
无 无 |
无 无 |
查看答案和解析>>
科目: 来源: 题型:
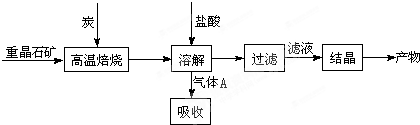
| 高温 |
| 高温 |
| c(Br-) |
| c(Cr-) |
| 高温 |
查看答案和解析>>
科目: 来源: 题型:
 硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)
硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)| 催化剂 | △ |
查看答案和解析>>
科目: 来源: 题型:
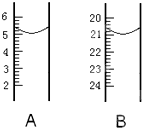 Ⅰ(1)某温度下,纯水中的c (H+)=4.0×10-7 mol/L,则此温度下纯水中的
Ⅰ(1)某温度下,纯水中的c (H+)=4.0×10-7 mol/L,则此温度下纯水中的查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com