
科目: 来源: 题型:选择题
| A. | 56g铁高温下与足量水蒸气充分反应转移电子数目为3NA | |
| B. | 100 g CaCO3和KHCO3混合固体中CO32-的数目为NA | |
| C. | 实验室用H2O2制备1mol O2转移的电子数为2NA | |
| D. | 标准状况下,2.24L CCl4含有的原子数为0.5NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 根据实验①可知溶液中不存CO32-、SiO32- | |
| B. | 该溶液中肯定存在NH4+、Fe2+ | |
| C. | 该溶液中至少含有4种离子 | |
| D. | 另取该溶液,加入适量氯水和淀粉溶液,若溶液显蓝色,即可确定该溶液中只含NH4+、Fe2+、Fe3+、SO42-、I- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 醋酸与CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | FeI2溶液中滴入过量溴水:2Fe2++2I-+2Br2═2 Fe3++I2+4Br- | |
| C. | NaHSO4溶液中滴入少量Ba(OH)2溶液:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+═Cl2+H2O↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 环氧乙烷的结构简式:C2H4O | B. | 中子数为16的磷原子:${\;}_{15}^{16}$P | ||
| C. | 氯原子的结构示意图: | D. | PC13的电子式: |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 明矾可用作净水剂 | 明矾能水解生成Al(OH)3 胶体 |
| B | FeCl3溶液可用于腐蚀铜制印刷电路 | FeCl3 溶液能与Cu反应 |
| C | SO2可用于漂白纸浆 | SO2 具有氧化性 |
| D | 酸性或碱性表示食物不宜放在铝锅中久置 | 铝能与酸或碱反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| B. | 0.5molC3H8分子中所含C-H共价键数为2NA | |
| C. | 标准状况下,22.4L乙醇完全燃烧所消耗的氧气分子数为3NA | |
| D. | 1molCH5+离子所含的电子数为11NA |
查看答案和解析>>
科目: 来源: 题型:解答题
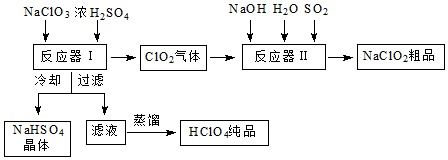
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 过氧化钠可用作潜艇里氧气的来源 | |
| B. | 新制的氯水需保存在棕色玻璃瓶中 | |
| C. | 二氧化氯具有强氧化性,可用于自来水的杀菌消毒 | |
| D. | 纯碱可用于治疗胃酸过多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com