
科目: 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O=2H++C1-+C1O- | |
| B. | 铝溶于过量的氨水:A1+2OH-+H2O=A1O2-+2H2↑ | |
| C. | 检验溶液中的 NH4+:NH4++OH-$\frac{\underline{\;加热\;}}{\;}$NH3↑+H2O | |
| D. | 用 H2S 处理含 Hg2+的废水:S2-+Hg2+=HgS↓ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用饱和的Na2SO4溶液使鸡蛋清发生盐析,进而分离、提纯蛋白质 | |
| B. | 淀粉和纤维素的组成都可用(C6H10O5)n表示,它们互为同分异构体 | |
| C. | 苯酚与苯甲酸都能发生加成反应、中和反应及氧化反应 | |
| D. | 食用植物油在烧碱溶液水解属于皂化反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
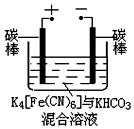 材料一:连二亚硫酸钠(Na2S2O4)是一种常用还原剂,俗称保险粉.工业制备方法如下:
材料一:连二亚硫酸钠(Na2S2O4)是一种常用还原剂,俗称保险粉.工业制备方法如下:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.6g甲烷含有的电子数为NA | |
| B. | 1L0.1mol•L-1NaHCO3溶液中含有的HCO3-数目为0.1NA | |
| C. | 1LpH=1的硫酸溶液中含有的H+数为0.2NA | |
| D. | 标准状况下,2.24LCO和CO2混合气体中含有的氧原子数为0.15NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.5mol/L100mL的FeI2溶液中,通入少量Cl2:2I-+Cl2=I2+2Cl- | |
| B. | 饱和的碳酸钠溶液中滴加少量稀盐酸:CO32-+H+=HCO3- | |
| C. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| D. | 次氯酸钠溶液中通入少量的SO2气体:2ClO-+SO2+H2O=SO32-+2HClO |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 42gC3H6中含有的共用电子对数目为 8NA | |
| B. | 由 6gCaCO3和 5gKHCO3组成的混合物中含有的碳原子数为 0.11NA | |
| C. | 标准状况下,22.4L 氯气和 56g 铁充分反应,转移的电子数为 3NA | |
| D. | 1L0.01mol•L-1KAl(SO4)2溶液中含有的阳离子数为 0.02NA |
查看答案和解析>>
科目: 来源: 题型:解答题
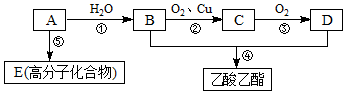
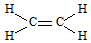 .
.查看答案和解析>>
科目: 来源: 题型:解答题
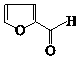 ).通常条件下,糠醛是无色油状液体,在空气中易变成黄棕色,能溶于丙酮、苯、乙醚等有机溶剂中,能与水部分互溶.糠醛用途广泛,如:用糠醛替代甲醛与苯酚在酸或碱催化下合成的酚醛树脂,可用作砂轮、砂纸、砂布的黏合剂;糠醛的氧化产物己二酸是合成锦纶纤维的重要单体;糠醛在以CuO-Cr2O3作为催化剂并加热加压的条件下,可制得糠醇(
).通常条件下,糠醛是无色油状液体,在空气中易变成黄棕色,能溶于丙酮、苯、乙醚等有机溶剂中,能与水部分互溶.糠醛用途广泛,如:用糠醛替代甲醛与苯酚在酸或碱催化下合成的酚醛树脂,可用作砂轮、砂纸、砂布的黏合剂;糠醛的氧化产物己二酸是合成锦纶纤维的重要单体;糠醛在以CuO-Cr2O3作为催化剂并加热加压的条件下,可制得糠醇(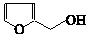 ),糠醇可以合成多种树脂;此外,糠醛还是合成香料、药物、染料等的原料.
),糠醇可以合成多种树脂;此外,糠醛还是合成香料、药物、染料等的原料.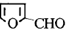 +H2$→_{加热加压}^{CuO-Cr_{2}O_{3}}$
+H2$→_{加热加压}^{CuO-Cr_{2}O_{3}}$ .
.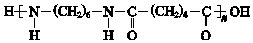
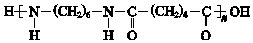 +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
科目: 来源: 题型:实验题
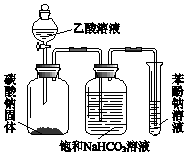 某同学欲用如图所示装置比较苯酚、乙酸、碳酸的酸性强弱,实验进行一段时间后,盛有苯酚钠溶液的试管中溶液变浑浊.
某同学欲用如图所示装置比较苯酚、乙酸、碳酸的酸性强弱,实验进行一段时间后,盛有苯酚钠溶液的试管中溶液变浑浊.查看答案和解析>>
科目: 来源: 题型:解答题
 某有机物由C、H、O三种元素组成,球棍模型如图所示:
某有机物由C、H、O三种元素组成,球棍模型如图所示: .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com