
科目: 来源: 题型:
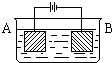 按右图的装置进行电解实验:A极是铜锌合金,B极为纯铜,电解质中含有足量的铜离子.通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.03g,则A合金中Cu、Zn原子个数比为( )
按右图的装置进行电解实验:A极是铜锌合金,B极为纯铜,电解质中含有足量的铜离子.通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.03g,则A合金中Cu、Zn原子个数比为( )查看答案和解析>>
科目: 来源: 题型:
 OCH2CH2OOC-
OCH2CH2OOC- -CO
-CO 的物质已成功实现了这种处理.试分析,若用CH3OH来处理它,得到的有机物可能是( )
的物质已成功实现了这种处理.试分析,若用CH3OH来处理它,得到的有机物可能是( )查看答案和解析>>
科目: 来源: 题型:
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com