
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:阅读理解
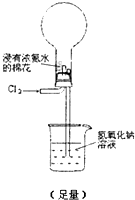 通过金属与盐溶液的置换反应可以比较金属还原性的强弱,通过非金属间的置换反应,也可以比较非金属氧化性的强弱.
通过金属与盐溶液的置换反应可以比较金属还原性的强弱,通过非金属间的置换反应,也可以比较非金属氧化性的强弱.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 以乙烯为原料,可以制备乙酸乙酯
以乙烯为原料,可以制备乙酸乙酯
 与足量金属钠反应的化学方程式
与足量金属钠反应的化学方程式

| 浓H2SO4 |
| △ |
| 浓H2SO4 |
| △ |
| 磷酸盐 |
查看答案和解析>>
科目: 来源: 题型:
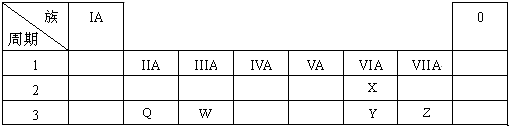
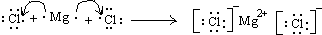

查看答案和解析>>
科目: 来源: 题型:



 或
或 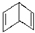 ,为验证其结构,取少量该液体,加入少量酸性高锰酸钾溶液,振荡,静置.若结构为
,为验证其结构,取少量该液体,加入少量酸性高锰酸钾溶液,振荡,静置.若结构为  ,其现象为
,其现象为 ,其现象为
,其现象为查看答案和解析>>
科目: 来源: 题型:
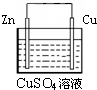 某同学用右图所示装置进行原电池实验.请回答:
某同学用右图所示装置进行原电池实验.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com