
科目: 来源: 题型:选择题
| A. | R(OH)3 | B. | R2O7 | C. | HRO3 | D. | H2R |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO2和SiO2 | B. | Na2O2和H2O2 | C. | NaCl和HCl | D. | CCl4和CS2 |
查看答案和解析>>
科目: 来源: 题型:选择题
 在结构化学中,可将晶体结构截分为一个个包含等同内容的基本单位,这个基本单位叫做晶胞.钙、钛、氧可以形成 如图所示的晶胞,则该物质的化学式可表示为( )
在结构化学中,可将晶体结构截分为一个个包含等同内容的基本单位,这个基本单位叫做晶胞.钙、钛、氧可以形成 如图所示的晶胞,则该物质的化学式可表示为( )| A. | Ca8TiO12 | B. | Ca4TiO6 | C. | Ca4TiO3 | D. | CaTiO3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 范德华力是决定由分子构成物质熔、沸点高低的惟一因素 | |
| B. | 范德华力与物质的性质没有必然的联系 | |
| C. | 范德华力能够影响物质的化学性质和物理性质 | |
| D. | 范德华力仅是影响物质部分物理性质的一种因素 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 单质的密度依次增大 | B. | 单质的熔点和沸点依次升高 | ||
| C. | Cl2可以从KI溶液中置换出I2 | D. | Br2可以从NaCl溶液中置换出Cl2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②③ | B. | ②③⑤ | C. | ③④ | D. | ①②④ |
查看答案和解析>>
科目: 来源: 题型:解答题
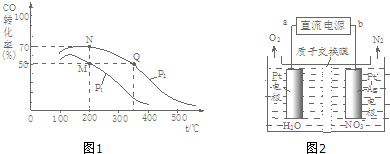
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com