
科目: 来源: 题型:选择题
| A. | 有单质生成的分解反应一定是氧化还原反应 | |
| B. | 氧化还原反应的本质是电子的得失或偏移 | |
| C. | 臭氧与氧气结构不同,二者之间的转化是氧化还原反应 | |
| D. | Cl-、I-、S2-等只有还原性,但也有不少阴离子有较强的氧化性 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
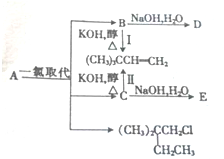 (1)A的分子式为C6H14,1molA完全燃烧消耗O29.5mol.
(1)A的分子式为C6H14,1molA完全燃烧消耗O29.5mol.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 醋酸的物质的量的浓度为0.1mol•L-1 | |
| B. | 醋酸溶液中由水电离出的:c(H+)=1.0×10-3 mol•L-1 | |
| C. | 反应后的溶液中:c(Na+)>c(CH3OO-)>c(OH-)>c(H+) | |
| D. | 反应后的溶液中:c(CH3COO-)+c(CH3OOH)=0.05mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:解答题
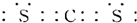
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 提高高锰酸钾的氧化能力,用浓盐酸酸化 | |
| B. | 抑制Fe2+ 的水解,用稀硝酸酸化 | |
| C. | 检验某卤代烃中是否含氯元素,先加HNO3酸化,再加AgNO3溶液检验. | |
| D. | 确认溶液中含有SO42- 时,先用过量盐酸酸化,再加BaCl2溶液检验. |
查看答案和解析>>
科目: 来源: 题型:解答题
 X、Y、Z、R为短周期元素,原子序数依次增大.X的一种单质是自然界中最硬的物质;Y的单质在空气中含量最高.Z 的氧化物是常见的两性氧化物;R 基态原子最外层成对电子的数目和未成对电子 的数目相等.
X、Y、Z、R为短周期元素,原子序数依次增大.X的一种单质是自然界中最硬的物质;Y的单质在空气中含量最高.Z 的氧化物是常见的两性氧化物;R 基态原子最外层成对电子的数目和未成对电子 的数目相等. 查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 常温下,甲、乙、丙三种单质均为气体 | |
| B. | 上述转化关系所涉及的化合物中有一种是电解质 | |
| C. | 上图所示的五个转化关系中,有三个是化合反应 | |
| D. | 上图所示的五个转化关系中,均为氧化还原反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{125a}{9V}$mol/L | B. | $\frac{125a}{18V}$mol/L | C. | $\frac{125a}{36V}$mol/L | D. | $\frac{125a}{54V}$mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com