
科目: 来源: 题型:选择题
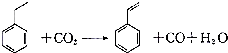
| A. | 分子中含有5个碳碳双键 | B. | 属于不含极性键的共价化合物 | ||
| C. | 分子式为C8H10 | D. | 通过加聚反应生成聚苯乙烯 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Y3X8分子中,极性键和非极性键的个数比为8:3 | |
| B. | Z和Q形成的两种化合物中只有一种属于酸性氧化物 | |
| C. | 25℃时,若WZX溶液中的C(OH-):C(H+)=1012,则该溶液的pH=13 | |
| D. | Q元素在自然界中不能以游离态存在 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||

查看答案和解析>>
科目: 来源: 题型:解答题
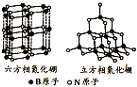 (1)短周期的元素a、b、c、d,原子序数依次增大.a原子的核外电子总数与其电子层数相同,b的基态原子各能级上排布的电子数相同,c的基态原子最高能层有3个未成对电子,d原子的最外层电子数为其内层电子数的3倍.
(1)短周期的元素a、b、c、d,原子序数依次增大.a原子的核外电子总数与其电子层数相同,b的基态原子各能级上排布的电子数相同,c的基态原子最高能层有3个未成对电子,d原子的最外层电子数为其内层电子数的3倍.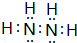 (填电子式).
(填电子式).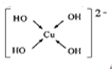 ;
;查看答案和解析>>
科目: 来源: 题型:选择题
| T/℃ | 30 | 40 | 50 |
| NH3的平衡浓度/(×10-6mol/L) | 4.8 | 5.9 | 6.0 |
| A. | 该反应的△H>0 | |
| B. | 常温下该反应的△S>0 | |
| C. | 反应在30℃、40℃时化学平衡常数分别为K1、K2,则K1<K2 | |
| D. | 在常温常压下,人工固氮比较容易进行 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径由小到大的顺序为:rW<rZ<rY | |
| B. | 简单离子氢化物的热稳定性Z>Y | |
| C. | X2W的沸点高于X2Z | |
| D. | 只含X、Y、W三种元素的化合物,不可能是离子化合物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向次氯酸钙溶液中通入SO2:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO | |
| B. | Fe3O4与稀硝酸反应:Fe3O4+8H+=2Fe2++Fe3++4H2O | |
| C. | 大理石溶于醋酸中:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | 溶液中FeBr2与等物质的量的Cl2反应:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+Br2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  制取纯净氢氧化亚铁 | B. | 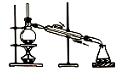 石油的蒸馏 | ||
| C. | 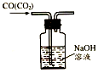 除去CO气体中的CO2气体 | D. | 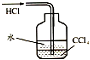 吸收HCl |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 明矾可用于自来水的杀菌消毒 | |
| B. | 钢铁在干燥的空气里不易被腐蚀,而在潮湿的空气里容易被腐蚀 | |
| C. | 生石灰能与水反应,可用来干燥氧气 | |
| D. | SiO2可用于制半导体材料,是利用了SiO2的导电性 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com