
科目: 来源: 题型:填空题
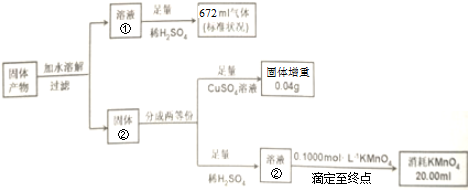
查看答案和解析>>
科目: 来源: 题型:填空题
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| 相应实验 | 实验器材(省略夹持装置) | |
| A | 氯化钠溶液的浓缩结晶 | 烧杯、玻璃棒、酒精灯 |
| B | 用盐酸除去硫酸钡中的少量碳酸铜 | 烧杯、漏斗、胶头滴管、滤纸 |
| C | 用浓硫酸配制0.5mol•L-1的溶液 | 烧杯、玻璃棒、胶头滴管、容量瓶 |
| D | 用溴水和CCl4除去NaBr溶液中的少量NaI | 烧杯、玻璃棒、胶头滴管、分液漏斗 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 太快而且太深的呼吸可导致碱中毒 | B. | 太快而且太深的呼吸可导致酸中毒 | ||
| C. | 太浅的呼吸可导致碱中毒 | D. | 太浅的呼吸可导致体内pH升高 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 升温 | B. | c(A)增大 | C. | C(C)降低 | D. | C(A)降低 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②④ | B. | ②③⑥ | C. | ④⑤⑥ | D. | ③⑤⑥ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 | |
| B. | 等物质的量的N2和CO所含原子数相同,质量相同 | |
| C. | 在标况下,22.4 L SO3所含氧原子为3NA | |
| D. | 1L 0.1 mol•L-1的乙酸溶液中H+数为0.1 NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该池可能是原电池,也可能是电解池 | |
| B. | 该池只能是原电池,且电解质溶液为硝酸 | |
| C. | 该池只能是电解池,且金属铜为该电解池的阴极 | |
| D. | 该池只能是电解池,电解质溶液可以是硫酸锌 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | (2)(3)(4)(5)(1) | B. | (4)(3)(2)(5)(1) | C. | (5)(2)(1)(3)(4) | D. | (5)(3)(1)(2)(4) |
查看答案和解析>>
科目: 来源: 题型:选择题
| 化学键 | H-H | Cl-Cl | Cl-H |
| 键能/(kJ•mol-1) | 436 | 243 | 431 |
| A. | 862 kJ•mol-1 | B. | 679 kJ•mol-1 | C. | 183 kJ•mol-1 | D. | -183 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com