
科目: 来源: 题型:选择题
| A. | 含53g碳酸钠的水溶液中含NA个CO32- | |
| B. | 0.1molOH-含NA个电子 | |
| C. | 1.8g重水(D2O)中含NA个中子 | |
| D. | 一定条件下的密闭容器中,足量N2与3mol H2充分反应可生成NH3 2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 位于短周期的X元素的阳离子与Y元素的阴离子具有相同的电子层结构,则两元素的最高正化合价一定是X<Y | |
| B. | 对于某元素的单质,若它的氧化性弱,那么它的还原性一定强 | |
| C. | 热稳定性:AsH3<PH3<H2O<HF | |
| D. | 最外层电子数较少的金属元素,一定比最外层电子数较多的金属元素活泼性强 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在河流入海处易形成三角洲 | |
| B. | 用微波手术刀进行外科手术,可使开到处的血液迅速凝固,减少失血 | |
| C. | 同一钢笔使用不同牌号的墨水容易堵塞 | |
| D. | 氢氧化铁固体溶于盐酸得澄清溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题
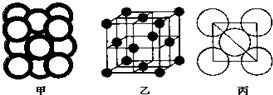
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲降低温度,乙不变 | |
| B. | 甲中加入0.1molHe,乙不改变 | |
| C. | 甲、乙提高相同温度 | |
| D. | 甲增加0.1mol H2,乙增加0.1mol I2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 由石墨比金刚石稳定可知:C(金刚石,s)=C(石墨,s)△H<0 | |
| B. | 强酸跟强碱反应放出的热量就是中和热 | |
| C. | 反应物的总能量低于生成物的总能量时,该反应一定不能发生 | |
| D. | 在101KPa、25℃时,1gH2完全燃烧生成气态水,放出120.9kJ热量,则氢气的燃烧热为241.8 kJ/mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碳酸钙溶于醋酸CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 锌片插入硝酸银溶液中Zn+Ag+═Zn2++Ag | |
| C. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| D. | 硫酸镁溶液和氢氧化钡溶液反应 SO42-+Ba2+═BaSO4↓ |
查看答案和解析>>
科目: 来源: 题型:选择题
| Nutrition Facts营养成分 500mL含量 | |
| 热量 710kJ | 碳水化合物 42g |
| 蛋白质 0g | 脂肪酸 0g |
| 维生素C 100mg | |
| 中国居民膳食营养素日推荐摄入量(RNI):维生素C 100mg | |
| A. | 1.14×10-3 mol•L-1 | B. | 0.2 mg•mL-1 | ||
| C. | 1.42×10-3 mol•L-1 | D. | 0.2 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com