
科目: 来源: 题型:选择题
| A. | 把CaO放入水中:CaO=Ca2++O2- | |
| B. | 加热NaHSO4至熔化:NaHSO4=Na2++H++SO42- | |
| C. | 把Mg(OH)2放入水中:Mg(OH)2=Mg2++2OH- | |
| D. | 把NaCl放入水中:NaCl=Na++Cl- |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1:2:3 | B. | 1:2:2 | C. | 6:3:2 | D. | 1:1:1 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3(aq)$\stackrel{△}{→}$Fe(OH)3(胶体) | |
| B. | Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{HCl(aq)}{→}$AlCl3 | |
| C. | FeS2$\frac{\underline{\;燃烧\;}}{\;}$SO3$\frac{\underline{\;H_{2}O\;}}{\;}$H2SO3 | |
| D. | 饱和NaCl(aq)$\frac{\underline{\;NH_{3}CO_{3}\;}}{\;}$NaHCO3$\stackrel{△}{→}$Na2CO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
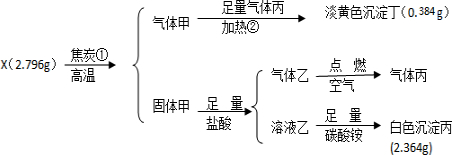
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:查看答案和解析>>
科目: 来源: 题型:解答题
 节能减排已经成为全社会的共识,浙江省在原先推行乙醇汽油的基础上,开始试点甲醇汽油(即在汽油中添加一定量的甲醇),根据检测的数据分析认为,若绍兴全市的100余万辆机动车全部使用甲醇汽油,一年内能减少有害气体(一氧化碳)排放将近100万吨.甲醇常利用煤气化过程中生成的CO和H2来制备:CO+2H2?CH3OH.
节能减排已经成为全社会的共识,浙江省在原先推行乙醇汽油的基础上,开始试点甲醇汽油(即在汽油中添加一定量的甲醇),根据检测的数据分析认为,若绍兴全市的100余万辆机动车全部使用甲醇汽油,一年内能减少有害气体(一氧化碳)排放将近100万吨.甲醇常利用煤气化过程中生成的CO和H2来制备:CO+2H2?CH3OH.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com