
科目: 来源: 题型:多选题
| A. | 测定溶液的pH | B. | 加入Ba(OH)2溶液 | ||
| C. | 加入盐酸 | D. | 加入品红溶液 | ||
| E. | 用蓝色石蕊试纸检测 |
查看答案和解析>>
科目: 来源: 题型:解答题
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
查看答案和解析>>
科目: 来源: 题型:解答题
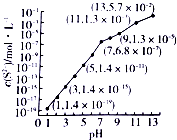 研究硫元素及其化合物的性质具有重要意义.
研究硫元素及其化合物的性质具有重要意义.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH4分子的球棍模型: | |
| B. | 中子数为146、质子数为92的铀原子${\;}_{92}^{146}$U | |
| C. | 氟化钠的电子式: | |
| D. | 正丁烷的结构简式:C4H10 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 仅含有碳和氢两种元素的有机物称为烃 | |
| B. | 凡是分子里含碳元素的化合物都属于有机物 | |
| C. | 甲烷可以使酸性高锰酸钾溶液褪色 | |
| D. | 甲烷与氯气混合光照一段时间后黄绿色变浅,因为发生了置换反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化石燃料燃烧和工业废气中的氮氧化物均是导致“雾霾天气”的元凶 | |
| B. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| C. | 含氟牙膏可以有效防止龋齿 | |
| D. | 化学药品着火,都要立即用水或泡沫灭火器灭火 |
查看答案和解析>>
科目: 来源: 题型:填空题
| K1 | K2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c(H+) | B. | c(X-) | C. | $\frac{c({H}^{+})}{c(HX)}$ | D. | $\frac{c(HX)}{c({H}^{+})}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com