
科目: 来源: 题型:阅读理解
| 实验步骤 | 预期现象和结论 | ① | 取少量上述漂白粉于试管中, 加入足量1mol.L-1的HCl,并将产生的气体导入澄清石灰水中 加入足量1mol.L-1的HCl,并将产生的气体导入澄清石灰水中 . |
(1)若澄清石灰水 若澄清石灰水未变浑浊 若澄清石灰水未变浑浊 ,则样品中不含碳酸钙 样品中不含碳酸钙 ;(2)若澄清石灰水 若澄清石灰水 变浑浊 若澄清石灰水 变浑浊 ,则样品中含有碳酸钙 样品中含有碳酸钙 |
② | 向实验①后的试管中滴入 几滴品红溶液,振荡 几滴品红溶液,振荡 . |
若 若品红褪色,则样品中含Ca(ClO)2 若品红褪色,则样品中含Ca(ClO)2 ;若 若品红不褪色,则样品中不含Ca(ClO)2 若品红不褪色,则样品中不含Ca(ClO)2 ; |
查看答案和解析>>
科目: 来源: 题型:
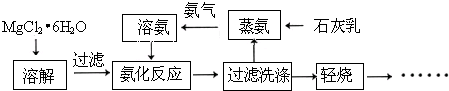
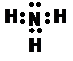
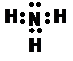
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:

| 106(d-b) |
| 44 |
| 106(d-b) |
| 44 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com