
科目: 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:选择题
已知常温下:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,则下列叙述正确的是
A.AgCl在饱和NaCl溶液中的KSP比在纯水中的KSP小
B.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明KSP(AgCl)<KSP(AgBr)
C.将0.001mol·L-1 AgNO3溶液滴入0.001mol·L-1 KCl和0.001mol·L-1 K2CrO4混合溶液中,先产生Ag2CrO4沉淀
D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:选择题
下列关于电解质溶液的叙述正确的是
A.常温下,在pH=7的醋酸钠和醋酸混合溶液中:c(CH3COO-)>c(Na+)
B.稀释醋酸溶液,溶液中所有离子的浓度均降低
C.在pH=5的氯化钠和稀硝酸的混合溶液中,c(Na+)=c(Cl-)
D.0.1mol·L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:填空题
已知2A2(g)+B2(g) 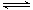 2C3(g);△H=-akJ·mol-1(a >0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C3的浓度为w mol·L-1,放出热量b kJ。请回答下列问题:
2C3(g);△H=-akJ·mol-1(a >0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C3的浓度为w mol·L-1,放出热量b kJ。请回答下列问题:
(1)比较a___________b填“>”、“=”、“<”)。
(2)若将反应温度升高到700℃,该反应的平衡常数将_____________(“增大”、“减小”或“不变”)。
(3)能说明该反应已经达到平衡状态的是
A.V(C3)=2V(B2) B.容器内气体压强保持不变
C.V逆(A2)=2V正(B2) D.容器内的气体密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是_____________。
A.及时分离出C3气体 B.适当升高温度
C.增大B2的浓度 D.选择高效的催化剂
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:填空题
(1)某温度时,水的离子积Kw=1×10-13,则该温度____________(填“大于”、“小于”或“等于”)25℃,其理由是_____________________。在此温度下,某溶液中由水电离出来的H+浓度为1×10-10mol/L,则该溶液的pH可能为 。
(2)若温度为25℃时,体积为Va、pH=a的H2SO4与体积为Vb、pH=b的NaOH混合,恰好中和。此溶液中各种离子的浓度由大到小的排列顺序是: 。
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:实验题
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
实验一:配制并标定醋酸溶液的浓度
取冰醋酸配制250mL0.2 mol·L-1的醋酸溶液,用0.2mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250mL0.2mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、____________和______________。
(2)为标定某醋酸溶液的准确浓度,用0.2000mol·L-1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
则该醋酸溶液的准确浓度为____________。(保留小数点后四位)
实验二: 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸溶液的pH,结果如下:
醋酸溶液浓度(mol·L-1) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
回答下列问题:
(1)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是__________。
(2)从表中的数据,还可以得出另一结论:随着醋酸溶液浓度的减小,醋酸的电离程度________(填“增大”“减小”或“不变”)。
实验三: 探究温度对醋酸电离程度的影响
请你设计一个实验完成该探究,请简述你的实验方案________________。
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:填空题
Ⅰ.常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量的浓度和混合液的pH如下表所示:
实验编号 | HA的物质的量浓度(mol·L-1) | NaOH的物质的量浓度(mol·L-1) | 混合后溶液的pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.12 | 0.1 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还弱酸? 。
(2)乙组混合溶液中离子浓度c(A-)和c(Na+)的大小关系是 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 。
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)= mol/L。
Ⅱ.某二元酸(分子式用H2B表示)在水中的电离方程式是:H2B=H++HB-;HB-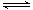 H++B2-
H++B2-
回答下列问题:
(5)在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是 。
A.c(B2-)+c(HB-)=0.1mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
查看答案和解析>>
科目: 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的作用,下列有关说法不正确的是
A.硅酸钠的水溶液俗称水玻璃,可用作木材防火剂
B.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量
C.含磷污水是很好的肥料,可灌溉庄稼,可直接排放到自然界水体中
D.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能杀菌消毒又能净水
查看答案和解析>>
科目: 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
已知吸热反应2CO(g)= 2C(s)+O2(g),设ΔH 和ΔS不随温度 而变,下列说法中正确的是
而变,下列说法中正确的是
A.低温下能自发进行 B.高温下能自发进行
C.任何温度下都能自发进行 D.任何温度下都不能自发进行
查看答案和解析>>
科目: 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
用下列装置能达到预期目的的是
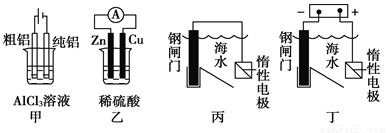
A.甲图装置可用于电解精炼铝
B.乙图装置可得到持续、稳定的电流
C.丙图装置利用了牺牲阳极的阴极保护法保护钢闸门不被腐蚀
D.丁图装置利用了外加电流的阴极保护法保护钢闸门不被腐蚀
查看答案和解析>>
科目: 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列与NA有关的说法正确的是
A.在反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,当得到标准状况下67.2 L Cl2时,反应中转移的电子数为6 NA
B.6.0 g SiO2晶体中含有的硅氧键数目为0.2 NA
C.标准状况下,22.4 L NO和11.2 L O2混合后气体的分子总数为NA
D.S2和S8的混合物共6.4 g,其中所含硫原子数一定为0.2 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com