
科目: 来源: 题型:
【题目】下列操作中正确的是 ( )
A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部。
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子一定能大量共存的是( )
A.在无色溶液中:NH4+、Fe2+、SO42-、CO32-
B.在含大量Ba2+的溶液中:NH4+、Na+、Cl-、OH-
C.在强碱溶液中:Na+、K+、Cl-、SO32-
D.在强酸性溶液中:K+、Fe2+、Cl-、CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.在一定条件下,反应A(g)+2B(s)![]() C(g)(正反应为吸热反应)达到平衡后,根据下列图像判断:
C(g)(正反应为吸热反应)达到平衡后,根据下列图像判断:


(1)增大压强,达到新平衡的是 (填图像对应的序号,下同)。A的转化率(填“增大”、“减小”、“不变”,下同) 。
(2)增大A的量,达到新平衡的是 ,此时A的转化率 。
Ⅱ.工业合成氨N2(g)+3H2(g)![]() 2NH3(g)反应过程中的能量变化如下图所示,据图回答下列问题:
2NH3(g)反应过程中的能量变化如下图所示,据图回答下列问题:

(1)该反应通常用活性铁作催化剂,加活性铁会使图中B点(填“升高”还是“降低”) ,理由是 。
(2)该反应平衡常数表达式为:K= ,增大氮气的量,K (填“增大”、“减小”、“不变”,下同)。
(3)一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的合理措施有 (填字母代号)。
a.高压 b.加入催化剂 c.增加N2的浓度 d.增加H2的浓度 e.分离出NH3
Ⅲ.在一定体积的密闭容器中,进行如下化学反应:其化学平衡常数K与温度t的关系如下:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答下列问题:
(1)该反应为 反应。(填“吸热”或“放热”)
(2)830℃,固定容器为2L的密闭容器中,放入混合物,其始浓度为c(CO) =0.1mol/L, c(H2O) =0.3mol/L,经3s后达到平衡,则平衡时CO的物质的量为 ;3s内CO2的平均反应速率为 。
(3)可以判断已知的可逆反应达到平衡状态的是 (填字母代号)。
a.容器内的压强不再变化
b.单位时间内生成amolCO2同时消耗amolCO
c.容器内生成的CO浓度与H2浓度相等
d.单位时间内生成amolCO2同时生成2amolCO
e.单位时间内生成amolCO2同时生成amolH2
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中发生如下反应:mA(g)+nB(s)![]() pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.5倍,下列说法错误的是( )
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.5倍,下列说法错误的是( )
A.m+n<p B.平衡向左反应方向移动
C.B的转化率降低 D.A的体积分数增加
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年10月17日7点30分,神舟十一号载人飞船发射升空。制造航天飞船的主要材料是铝,工业上制铝时用冰晶石(Na3AlF6)做助熔剂,冰晶石制备流程有如下两种:
方案一:以纯碱和萤石(CaF2)为主要原料
![]()
方案二:以碳酸氢铵和六氟合硅酸为主要原料

(1)方案一中B可作为建筑材料,化合物A 是________,写出由C制备冰晶石的化学方程式____________________________。
(2)方案二中反应1产生的气体是_____________,反应2后滤液中主要成分的用途_________。
(3)方案二中反应2化学方程式________________________。
(4)工业电解制铝的阴极反应式为_________________,以石墨为电极维持电流180千安电解5小时生成铝270千克,则电流效率η(η=实际产量/理论产量)为_______。(法拉第常数F = 96500 C·mol-1)
查看答案和解析>>
科目: 来源: 题型:
【题目】氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,他们应用广泛。
(1)N2O是人类最早应用于医疗的麻醉剂之一。它可由NH4NO3在加热条件下分解产生,此反应的化学方程式为___________。已知N2O与CO2分子具有相似的结构,试画出N2O的结构式_______。
(2)N2O4可作火箭高能燃料N2H4的氧化剂。
已知:2NO2(g)![]() N2O4(g) △H =-akJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;
N2O4(g) △H =-akJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;
N2(g)+2O2(g)=2NO2(g) △H =+ckJ·mol-1;(a、b、c均大于0)。
写出气态腁在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式___________。
(3)平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数(例如p(NO2)=p总×x(NO2))。写出反应2NO2(g)![]() N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式________(用p总、各气体物质的量分数x表示)。
N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式________(用p总、各气体物质的量分数x表示)。
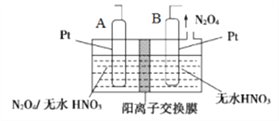
(4)新型绿色硝化剂N2O5可以N2O4为原料用电解法制备,实验装置如图所示。则电极B接直流电源的____极,电解池中生成N2O5的电极反应式为_____________。
(5)可用氨水吸收NO2、O2生成硝酸铵,写出该反应的离子方程式_____________。
已知25℃时NH3·H2O的电离常数Kb=2×10-5,向500ml0.1mol·L-1硝酸铵溶液中通入标准状况下至少____ml氨气,使溶液呈中性(溶液的体积变化忽略不计)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于生物体内水和无机盐的叙述,错误的是
A. 是细胞中能源物质之一
B. 哺乳动物血液中钙离子含量过少会引起抽搐
C. 细胞内的自由水是生化反应的重要介质
D. 铁是合成血红蛋白的原料
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于硫酸的说法正确的是( )
A.浓硫酸有脱水性,故可用做干燥剂
B.浓硫酸有强酸性,故能与金属活动顺序氢后的金属反应
C.硫酸的酸性比盐酸强,利用复分解反应用硫酸可以制盐酸
D.由于浓硫酸具强氧化性,因此不能干燥硫化氢和碘化氢气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com