
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 (2012?闸北区一模)碳酸钠和碳酸氢钠在生产、生活中都有重要的应用.现有3.58g Na2CO3和NaHCO3固体混合物,将其制成溶液后,边搅拌边逐滴滴加80.0mL 1.0mol/L盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为896mL(设气体全部逸出,下同).(1)通过计算可知上述反应中
(2012?闸北区一模)碳酸钠和碳酸氢钠在生产、生活中都有重要的应用.现有3.58g Na2CO3和NaHCO3固体混合物,将其制成溶液后,边搅拌边逐滴滴加80.0mL 1.0mol/L盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为896mL(设气体全部逸出,下同).(1)通过计算可知上述反应中查看答案和解析>>
科目: 来源: 题型:
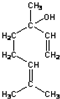
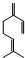 ,一分子该物质与一分子溴发生加成反应的产物(只考虑位置异构)理论上最多有
,一分子该物质与一分子溴发生加成反应的产物(只考虑位置异构)理论上最多有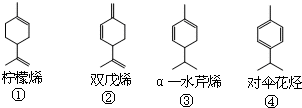
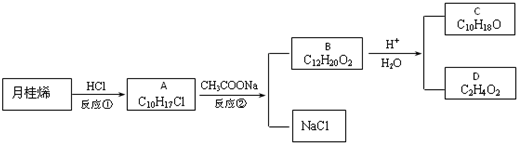
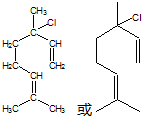




查看答案和解析>>
科目: 来源: 题型:
喹啉是一种重要的杂环化合物,它存在于多种药物之中,将萘(相对分子质量为128)分子中的一个碳原子(α位)换成一个氮原子,即得喹啉,其相对分子质量是
A.127 B.129 C.130 D.131
查看答案和解析>>
科目: 来源: 题型:
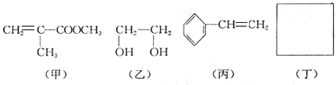
| 稀硫酸 |
| △ |
| 一定条件 |
| 试剂X |
| NaOH溶液 |
| △ |
| 一定条件 |
| 一定条件 |


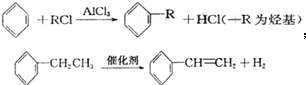


查看答案和解析>>
科目: 来源: 题型:阅读理解

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com