
科目: 来源: 题型:
【题目】I.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定装置如图

(1)图中A的名称是:_____________________________
(2)若实验过程中酸碱添加过慢,所得△H将________(填:偏大、偏小或者无影响)
(3)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 30.1 |
2 | 27.0 | 27.4 | 27.2 | 33.3 |
3 | 25.9 | 25.9 | 25.9 | 29.8 |
4 | 26.4 | 26.2 | 26.3 | 30.4 |
近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g℃).则中和热△H=_____________(取小数点后一位).
II.为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列的实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。

(4)请完成此实验设计,其中:V6=________,V8=___________
(5)该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,请分析主要原因________________________。
III.利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42-+2H+=Cr2O72-+H2O Ba2++CrO42-=BaCrO4↓
步骤Ⅰ:移取xmL一定物质的量浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂
步骤Ⅱ:移取ymL BaCl2溶液于锥形瓶中,加入xmL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用bmol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
(6)BaCl2溶液的浓度为___________mol·L-1,若步骤Ⅱ中滴加盐酸时有少量盐酸滴至锥形瓶外,Ba2+浓度测量值将______________(填“偏大”或“偏小”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质的性质与应用具有对应关系的是
A.铝易发生钝化,可用作导电材料B.炭具有还原性,可用于冶炼金属
C.Fe熔点高,可用作食品脱氧剂D.N2难溶于水,可用作保护气
查看答案和解析>>
科目: 来源: 题型:
【题目】相同条件下,下列关于物质性质的比较中,不正确的是
A.密度:水 > 苯B.沸点:乙二醇 > 乙醇
C.与Br2反应的活性:苯 > 苯酚D.在水中的溶解度:乙醛 > 溴乙烷
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于营养物质的说法中,不正确的是
A.麦芽糖是具有还原性的二糖B.油脂属于天然有机高分子
C.蛋白质水解的最终产物是氨基酸D.食用新鲜蔬菜和水果可补充维生素C
查看答案和解析>>
科目: 来源: 题型:
【题目】质量分数为a%,物质的量浓度为c molL﹣1的NaCl溶液,蒸发溶剂,恢复到原来的温度,若物质的量浓度变为2c molL﹣1 , 则质量分数变为(蒸发过程中没有晶体析出,且NaCl溶液的密度大于1g/mL)( )
A.等于2a%
B.大于2a%
C.小于2a%
D.无法确定
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)1L 0.05mol/LNaHCO3溶液与足量的盐酸完全反应,放出10kJ的热量,写出此反应的热化学方程式________________________________________________________
(2)写出明矾溶液与碳酸氢钠溶液反应的离子方程式______________
(3)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3-![]() H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象_________
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象_________
(4)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl,利用Ag+与CrO42生成砖红色沉淀,指示到达滴定终点。当溶液中Cl恰好沉淀完全(浓度等于1.0×105mol·L1)时,溶液中c(Ag+)为_______mol·L1,此时溶液中c(CrO42)等于__________mol·L1。(已知Ag2 CrO4、AgCl的Ksp分别为2.0×1012和2.0×1010)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列判断错误的是
A. 碘升华——分子间作用力被破坏
B. HCl气体溶于水——共价键被破坏
C. NaCl晶体溶于水——离子键被破坏
D. 氢氧化钠熔化——离子键和共价键被破坏
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各溶液中,Na+浓度最大的是
A. 8 L 0.2mol/L的Na2SO4溶液 B. 8 L0.15mol/L的Na3PO4溶液
C. 10 L0.1 mol/L的Na2CO3溶液 D. 2 L 0.5mol/L的NaCl溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用有机含碘(主要以I2和IO3-的形式存在)废水制备单质碘的实验流程如下:

已知:碘的熔点为113℃,但固态的碘可以不经过熔化直接升华。下列说法错误的是
A. 操作①和③中的有机相从分液漏斗下端放出
B. 操作②中发生反应的离子方程式为2IO3- +5SO32-+2H+=I2+5SO42-十H2O
C. 操作④中用到的玻璃仪器仅需温度计、球形冷凝管、酒精灯、接引管及锥形瓶
D. 操作⑤可用如图所示的水浴装置进行
查看答案和解析>>
科目: 来源: 题型:
【题目】氧和氮是大气的主要成分,氮的化合物在工业上均有重要的应用。
(1)根据下列反应写出由热化学循环在较低温度下由水分解制备氢气的热化学方程式:________________
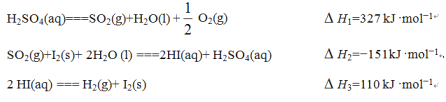
(2)在恒容密闭容器中,发生反应N2(g)+3H2(g) ![]() 2NH3(g),下列说法可以证明反应已达到平衡状态的是__________________。(填序号)
2NH3(g),下列说法可以证明反应已达到平衡状态的是__________________。(填序号)
①单位时间内生成n molN2的同时生成2n molNH3
②1个N≡N键断裂的同时,有6个N—H键形成
③1个N≡N键断裂的同时,有3个H—H键形成
④混合气体的密度不再改变的状态 ⑤混合气体的压强不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态。
为提高H2的转化率,实际生产中宜采取的措施有________(填字母)。
A.及时移出氨 B.最适合催化剂活性的适当高温
C.适当增大压强 D.循环利用和不断补充氮气
E.减小压强 F.降低温度
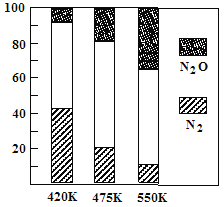
(3)电厂烟气脱氮的主反应①: 4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g),副反应②: 2NH3(g)+8NO(g)
5N2(g)+6H2O(g),副反应②: 2NH3(g)+8NO(g)![]() 5N2O(g)+3H2O(g)。平衡混合气中N2与N2O含量与温度的关系如图,请解释在400K~600K时,平衡混合气中这两种气体的含量随温度的变化而改变的原因是_____________________________
5N2O(g)+3H2O(g)。平衡混合气中N2与N2O含量与温度的关系如图,请解释在400K~600K时,平衡混合气中这两种气体的含量随温度的变化而改变的原因是_____________________________
(4)肼(N2H4)是一种重要的化工原料,既可用于制药,又可用作火箭燃料。向2 L的恒容密闭容器中充入2mol N2H4,发生反应N2H4(g)![]() N2(g)+2H2(g),
N2(g)+2H2(g),![]() (用x表示)与时间的关系如图1所示,则该温度下,此反应的平衡常数K=_______________。
(用x表示)与时间的关系如图1所示,则该温度下,此反应的平衡常数K=_______________。
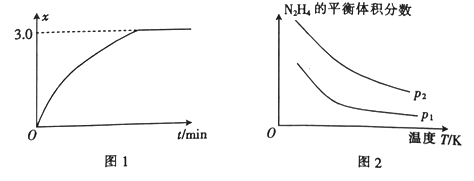
肼在另一条件下也可达到分解平衡,同时生成两种气体,且其中一种气体能使湿润的红色石蕊试纸变蓝。图2为平衡体系中肼的体积分数与温度、压强的关系,则p2_______ (填“大于”或“小于”) p1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com