
科目: 来源: 题型:
【题目】在400℃、101 kPa时,NO2(g) +CO(g) ![]() NO(g) + CO2(g) 反应过程的能量变化如下图所示。
NO(g) + CO2(g) 反应过程的能量变化如下图所示。
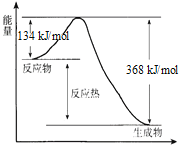
反应过程
(1)该反应是_____________(填“吸热”或“放热”)反应。
(2)该反应的热化学方程式为_____________。
(3)改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是_____________。
a.浓度 b.压强 c.温度 d.催化剂
(4)反应体系中加入催化剂对反应热是否有影响?____(填“是”或“否”),原因是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】在进行中和热的测定中,下列操作错误的是( )
A. 反应前酸、碱溶液的温度要相同
B. 测量溶液的温度计要一直插在溶液中
C. 为了使反应均匀进行,可以向酸(碱)中分次加入碱(酸)
D. 为了使反应更完全,可以使酸或碱适当过量
查看答案和解析>>
科目: 来源: 题型:
【题目】共价键、金属键、离子键和分子间作用力都是构成物质微粒间的不同相互作用力,含有上述中的三种相互作用力的晶体是( )
A. SiO2晶体 B. CCl4晶体 C. NaCl晶体 D. 石墨晶体
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如右图所示,
由图中数据分析:
(1)该反应的化学方程式:_____________;
(2)反应开始至2min末,X的反应速率为_________;
(3)3min后图中曲线所表示的含义是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】中和热的测定实验中取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
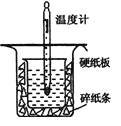
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是__________,除此之外,装置中的一个明显错误是_____________。
(2)若改用60mL 0.25mol·L-1 H2SO4和50mL 0.55mol·L-1 NaOH溶液进行反应与上述实验相比,所放出的热量_______(填“相等”或“不相等”)
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
2 | 27.0 | 27.4 | 27.2 | 32.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
4 | 26.4 | 26.2 | 26.3 | 29.8 |
(3)近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃),通过以上数据计算中和热ΔH=_______( 结果保留小数点后一位)。
(4)上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)________。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
查看答案和解析>>
科目: 来源: 题型:
【题目】[2017江苏]化合物H是一种用于合成γ-分泌调节剂的药物中间体,其合成路线流程图如下:
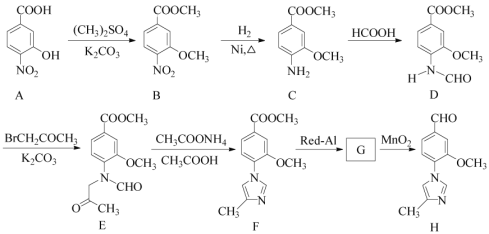
(1)C中的含氧官能团名称为_______和__________。
(2)D→E的反应类型为__________________________。
(3)写出同时满足下列条件的C的一种同分异构体的结构简式:_____________________。
①含有苯环,且分子中有一个手性碳原子;②能发生水解反应,水解产物之一是α-氨基酸,另一水解产物分子中只有2种不同化学环境的氢。
(4)G 的分子式为C12H14N2O2,经氧化得到H,写出G的结构简式:__________________。
(5)已知: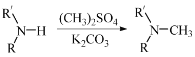 (R代表烃基,R'代表烃基或H)
(R代表烃基,R'代表烃基或H)
请写出以![]() 、
、![]() 和(CH3)2SO4为原料制备
和(CH3)2SO4为原料制备![]() 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目: 来源: 题型:
【题目】硅及其化合物在材料领域中应用广泛。下列叙述中,正确的是
A. 晶体硅是良好的半导体材料 B. 硅是地壳中含量最多的元素
C. SiO2和酸,碱都可以反应,故为两性氧化物 D. 硅是生产光导纤维的主要原料
查看答案和解析>>
科目: 来源: 题型:
【题目】强酸与强碱的稀溶液发生中和反应热效应表示为:H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3KJmol﹣1分别向1L0.5molL﹣1的Ba(OH)2的溶液中加入①浓硫酸;②稀硝酸;③稀醋酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是()
A.△H1>△H2>△H3B.△H1<△H2<△H3
C.△H1>△H2=△H3D.△H1=△H2<△H3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是:
A. 能量较高、有可能发生有效碰撞的分子称为活化分子
B. 活化分子的平均能量与所有分子的平均能量之差称为活化能
C. 催化剂能参与反应,可降低原反应所需活化能
D. 非活化分子也有可能发生有效碰撞
查看答案和解析>>
科目: 来源: 题型:
【题目】氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下表:
温度/℃ | 200 | 300 | 400 | 500 | 600 |
氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
请回答:
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是_______。
(2)在一定温度下,将2molN2和6molH2通入到体积为2L的密闭容器中,发生反应N2+3H2![]() 2NH3,2min达到平衡状态时,H2转化率是50%,该温度下的平衡常数K=_______________(结果用最简分数表示);欲使K增大,可以采取的措施是______。
2NH3,2min达到平衡状态时,H2转化率是50%,该温度下的平衡常数K=_______________(结果用最简分数表示);欲使K增大,可以采取的措施是______。
(3)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是______(选填序号字母)
a.及时分离出NH3 b.升高温度 c.增大压强 d.使用催化剂
(4)NH3能分解为N2和H2,在相同条件下,测得分解后混合气体密度为分解前的2/3,则氨的分解率为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com