
科目: 来源: 题型:
【题目】下列与无机盐的功能无关的是( )
A. 是某些重要的复杂化合物的组成成分 B. 维持细胞的形态和功能
C. 维持生物体的生命活动 D. 是细胞中的能源物质之一
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各晶体按熔点由低到高的顺序排列正确的是( )
A.H2、N2、O2、Cl2
B.HF、HCl、HBr、HI
C.Be、Mg、Ca、Sr
D.Na2O、Na2S、Na2Se
查看答案和解析>>
科目: 来源: 题型:
【题目】向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液.下列图象中,能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量)( )
A.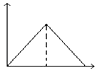
B.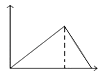
C.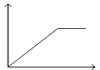
D.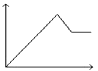
查看答案和解析>>
科目: 来源: 题型:
【题目】在酸性溶液中,能共存的离子组是( )
A. Na+ 、K+、SO42-、HCO3 B. Fe2+、K+、SO42-、NO3
C. Ba2+、 K+、Cl、 NO3 D. Fe3+、K+、SCN-、Cl
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,已知:①C+、D3+均与E的气态氢化物分子含有相同的电子数;A2-、B-与B的气态氢化物分子含有相同的电子数;②A单质在空气中燃烧产生气体R;③B的气态氢化物与E的气态氢化物相遇时有白烟生成。
请回答下列问题:
(1)元素A在元素周期表中的位置是__________
(2)A、B、C、D的简单离子半径从大到小顺序为______________(用离子符号表示)
(3)B的气态氢化物与E的气态氢化物相遇时生成白烟的电子式为_________,其中所含化学键类型为_____________
(4)D的最高价氧化物的水化物与C的最高价氧化物的水化物反应的离子方程式为_____
(5)A元素和B元素以原子个数比1:1形成化合物Q,Q的结构式为________
己知Q是种黄色油状液体,常温下遇水易反应,产生R气体,易溶液出现浑浊,请写Q与水反应的化学方程式___________
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出). 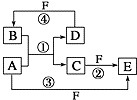
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,B为无色气体,则A在周期表中的位 置为第周期族,反应④的化学方程式 .
(2)若A是常见的变价金属的单质,D、F均为气态单质,且F为黄绿色,光照条件下D与F会发生反应.已知反应①和②均在水溶液中进行,则检验C中阳离子的操作步骤是: .
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,D是制取集成电路的主要原料,则B在通讯领域用来作 , 反应①的化学方程式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】氮的氧化物是主要的空气污染物,目前消除氯氧化物污染的方法有多种。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1(Ⅰ)
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1(Ⅱ)
H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1(Ⅲ)
①写出CH4 (g)与NO2 (g)反应生成N2 (g) ,CO2(g)和H2O(l)的热化学方程式:________
②为研究不同条件下对上述反应( Ⅱ )的影响,在恒温条件下,向2 L 的恒容密闭容器中加入0.2mol CH4和0.4mol NO2,10min反应(Ⅱ)达到平衡,测得l0min内v(NO)=5×10-3mol/(L·min),则平衡后n(CH4)=___mol,NO2的转化率a1=_________.其它条件不变,反应在恒压条件下进行,平衡时NO2的转化率a2____a1(填“大于” 小于”或“ 等于” )。
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g)![]() N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T℃)条件下反应,反应进行到不同时间测得各物质的浓度如下
N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T℃)条件下反应,反应进行到不同时间测得各物质的浓度如下
时间 浓度(mol/L) 物质 | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
①不能作为判断反应达到化学平衡状态的依据 是_________
A.容器内CO2的浓度保持不变
B.v正(N2)= v正(NO)
C.混合气体的平均相对分子质量保持不变
D.混合气体的密度保持不变
E.容器内压强保持不变
②在T℃时.该反应的平衡常数为_______ (保留两位小数);
③在30 min,改变某一条件,反应重新达到平衡,则改变的条件是________。
(3)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变成CO2和N2, 研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.如图表示在其他条件不变时,反应:2CO(g)+2NO(g)![]() N2(g)+2CO2(g) 中NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
N2(g)+2CO2(g) 中NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。

①该反应的ΔH____0(填“>”或“<”)。
②若催化剂的表面积S1 >S2,在图中画出c(NO)在T1、S2条件下达到平衡过程中的变化曲线。____
查看答案和解析>>
科目: 来源: 题型:
【题目】主族元素的阳离子和阴离子都具有稀有气体元素原子的结构特征,阳离子比阴离子少两个电子层的离子化合物是( )
A. MgCl2 B. NaBr C. HCl D. NaI
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关生物体内的化学元素的叙述,不正确的是
A. N是生长激素和ATP的组成元素
B. Mg是动物骨骼的重要组成元素
C. 血液中Ca2+含量低于正常值时,会导致肌肉抽搐
D. 缺Fe会导致贫血的原因是Fe是血红蛋白的组成元素
查看答案和解析>>
科目: 来源: 题型:
【题目】将镁、铝的混合物共0.2mol,溶于200mL 4molL﹣1的盐酸溶液中,然后再滴加2molL﹣1的NaOH溶液.请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量m 随加入NaOH溶液的体积V变化情况如图所示.当V1=160mL时,则金属粉末中n (Al)=mol 
(2)0~V1段发生的反应的离子方程式为;
(3)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=mL;
(4)若镁、铝的混合物仍为0.2mol,其中镁粉的物质的量分数为a,改用200mL 4molL﹣1的硫酸溶解此混合物后,再加入840mL 2molL﹣1的NaOH溶液,所得沉淀中无Al(OH)3 , 则a的取值范围为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com