
科目: 来源: 题型:
【题目】现有以下几种措施:①对燃烧煤时产生的尾气进行脱硫处理②少用原煤做燃料③燃煤时鼓入足量空气④开发清洁能源。其中能减少酸雨产生的措施是
A. ①②③ B. ②③④
C. ①②④ D. ①③④
查看答案和解析>>
科目: 来源: 题型:
【题目】两种气态烃的混合物共2.24L(标准状况),完全燃烧后得3.36L〔标准状况)二氧化碳和3.6g的水,下列说法中正确的是( )
A.混合气体中一定含有乙烯
B.混合气体中一定含有甲烷
C.混合气体中一定含有丙烯
D.混合气体一定是由烷烃和烯烃构成的混合物
查看答案和解析>>
科目: 来源: 题型:
【题目】铁元素及其化合物与人类的生产生活息息相关,试回答下列问题:
(1)有科学家提出可利用FeO吸收和利用CO2,相关热化学方程式如下:
6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △H=-76.0kJ/mol,
C(s)+2H2O(g)=CO2(g)+2H2(g) △H=113.4kJ/mol;
写出FeO(s)和H2O(g)生成Fe3O4(s)和H2(g)的热化学方程式:___________。
(2)以H2、O2、熔融Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如图所示,其中P端通入CO2.
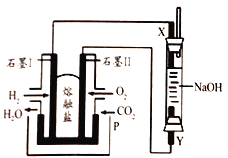
①石墨II电极的名称是______(填“正极”或“负极”);
石墨I电极上的电极反应式为__________。
②Y电极的电极材料是_________;X电极的电极反应式为_________。
通电一段时间后,若右侧玻璃管中产生1molFe(OH)2白色沉淀,理论上P端通入的CO2在标准状况下的体积至少为_____L。
查看答案和解析>>
科目: 来源: 题型:
【题目】在100℃时,将0.40mol的二氧化氮气体充入2L真空的密闭容器中,发生反应: 2NO2(g)![]() N2O4(g) △H=-24.4kJ/mol,每隔一段时间对该容器内的物质进行分析,得到数据如表所示:
N2O4(g) △H=-24.4kJ/mol,每隔一段时间对该容器内的物质进行分析,得到数据如表所示:
时间(s) | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4 )/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)从反应开始至20s时,二氧化氮的平均反应速率为_______mol·L-1·s-1。
(2)n3=______,100℃时该反应的平衡常数为______(保留一位小数)。平衡后,若升高温度,该反应的化学平衡常数将_______(填“增大”、“减小”或“不变”)。
(3)下述各项能说明反应达到平衡状态的是_______(填序号)。
a.v正(N204)= 2v逆(NO2) b.体系颜色不变
c.气体平均相对分子质量不变 d.气体密度不变
(4)达到平衡后,分别在80s、120s、140s时只改变一个条件,v正、v逆发生如下图所示变化;则80s时改变的条件可能是________。

(5)若在相同情况下,最初向该容器中充入的是四氧化二氮气体,要达到上述同样的平衡状态,四氧化二氮的起始浓度是_______mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度的体积一定的密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应:A(s)+2B(g)C(g)+D(g)已达到平衡状态( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④气体的总物质的量 ⑤混合气体的平均相对分子质量 ⑥物质C的百分含量 ⑦各气体的物质的量.
A.②③⑤⑥⑦
B.①②③⑥⑦
C.②③④⑤⑥
D.①③④⑤⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】用铂电极电解某金属的硫酸盐(XSO4)溶液,当阳极上收集到1.12L气体(标准状况,忽略气(体溶解)时,阴极质量增加6.4g,下列判断不正确的是
A. 该金属是Cu
B. 电路中有0.1mol电子通过
C. 电解后溶液的pH降低
D. 向电解后的溶液中加入0.1molCuO可使溶液恢复电解前的状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com