
科目: 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.石灰乳与碳酸钠溶液反应:Ca2++CO32﹣=CaCO3↓
B.NH4HSO3溶液与足量的氢氧化钠溶液混合加热:NH4++HSO3﹣+2OH﹣ ![]() NH3↑+SO32﹣+2H2O
NH3↑+SO32﹣+2H2O
C.酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3﹣+5I﹣+3H2O=3I2+6OH﹣
D.AgNO3溶液中加入过量的氨水:Ag++NH3?H2O=AgOH↓+NH4+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验误差分析正确的是( )
A.用湿润的pH试纸测稀碱液的pH,测定值偏大
B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D.测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏大
查看答案和解析>>
科目: 来源: 题型:
【题目】氮元素可以形成许多化合物,在我们生活生产中有广泛的应用。
(1)与NF3分子互为等电子体的分子为。
(2)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图甲。
①写出Fe3+的基态电子排布式。
②写出该反应的化学方程式:。


甲 乙 丙
(3)维生素B4结构如图乙,则1 mol维生素B4分子中含有σ键的数目为mol。
(4)配合物丙的结构见图,丙中含有(填序号);
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
丙中碳原子的杂化方式有。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( ) 
A.该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol/L
B.1 mol Mg与足量该硫酸反应产生2 g氢气
C.配制250 mL 1.0 mol/L的稀硫酸需取该硫酸约13.6mL
D.该硫酸溶液可作H2S的干燥剂
查看答案和解析>>
科目: 来源: 题型:
【题目】保护环境是每个公民的责任。下列做法:①推广使用无磷洗涤剂②城市生活垃圾分类处理③推广使用一次性筷子④推广使用清洁能源⑤过量使用化肥、农药⑥推广使用无氟冰箱。其中有利于保护环境的是( )
A.①②④⑤B.①②④⑥C.②③④⑥D.③④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
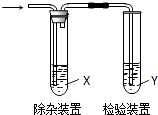
【题目】用如图所示装置检验乙烯时不需要除杂的是( )
乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
C | C2H5OH与浓H2SO4加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | C2H5OH与浓H2SO4加热至170℃ | NaOH溶液 | Br2的CCl4溶液 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上可以采用热还原法制备金属镁(镁沸点为1107℃,熔点是648.8℃)。
(1)将碱式碳酸镁[4MgCO3·Mg(OH)2·5H2O]和焦炭按一定比例混合,放入真空管式炉中先升温至500℃保持一段时间,然后升温至1450℃反应制得镁。
①用碳还原法制备金属镁需要在真空中而不在空气中进行,其原因是。
②焦炭与碱式碳酸镁的物质的量的比值不同对镁的还原率有较大影响,结果如图。当比值大于15∶1时,还原率下降的原因可能是。
③碱式碳酸镁分解如图所示,写出在1450℃反应制得镁的化学反应方程式。

(2)工业上可以采用MgCl2溶液和Na2CO3溶液混合制备碱式碳酸镁,写出反应离子方程式。反应采用68℃,温度不宜高于68℃的原因是。
(3)工业采用电解MgCl2溶液产生Mg(OH)2 , 如图。然后用Mg(OH)2悬浊液吸收烟气中的二氧化碳,减少二氧化碳的排放同时产生碱式碳酸镁。该电池的阴极电极反应式为。电解时还得到副产物为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com