
科目: 来源: 题型:
【题目】NA代表阿伏伽德罗常数,下列说法正确的是( )
A.0.1 molNa2O2与足量的CO2充分反应转移的电子数为0.2NA
B.常温常压下,18g H2O 所含的中子数为8NA
C.0.1 mol铁在0.1 mol Cl2中充分燃烧,有0.3NA个电子转移
D.将含0.1 mol FeCl3的饱和溶液制成胶体后,生成的Fe(OH)3胶粒数目为0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】葡萄糖的分子式为C6H12O6 , 下列关于葡萄糖的说法错误的是( )
A.葡萄糖由碳、氢、氧三种元素组成
B.葡萄糖分子中氢、氧原子个数比为2∶1
C.葡萄糖的相对分子质量为188
D.葡萄糖在人体内氧化可提供能量
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B两种元素为同一族第三周期和第四周期元素,若A元素的原子序数为x,则B元素的原子序数可能为( )
①x+2 ②x+8 ③x+18 ④x+32
A. ①③B. ②④C. ②③D. ①②
查看答案和解析>>
科目: 来源: 题型:
【题目】白磷是制备高纯度磷酸、烟幕弹、燃烧弹等的重要原料,工业上制备白磷的原理之一为4Ca5 (PO4)3F+21Si02+30C3P4+20GaSiO3+30CO↑+SiF4 , 回答相关问题:
(1)基态磷原子的价层电子排布图为 , 上述反应涉及的第二周期元素中第一电离能由大到小的顺序为(用元素符号表示).
(2)上述物质中,中心原子杂化轨道类型为sp3的分子有 , SiF4分子构型为 . 若不考虑C的晶体类型,则上述反应过程消失的晶体类型为 .
(3)碳、硅同一主族,CF4沸点比SiF4低的原因是;碳能形成π键而硅难形成π键的主要原因是 .
(4)图1为硫、磷元素形成的一种分子,分子中每个原子最外层均达到8电子稳定结构,该化合物的分子式为 , 若其晶体中分子的堆积方式与干冰相同,则晶体中每个分子的配位数是 . 
(5)碳、硅两种元素形成的一种高硬度化合物的晶胞如图2所示,若该化合物的密度为ρgcm3 , 晶胞参数为a pm,则阿伏伽德罗常数为mol﹣1 .
查看答案和解析>>
科目: 来源: 题型:
【题目】有关糖类的叙述中正确的是( )
A.糖类是具有甜味的物质
B.糖类是具有Cn(H2O)m通式的物质
C.糖类是含有醛基的物质
D.糖类物质是绿色植物光合作用的产物,是动植物所需能量的主要来源
查看答案和解析>>
科目: 来源: 题型:
【题目】氨气、尿素[CO(NH2)2]、Na2CO3均是重要的化工原料和产品,如图是某化工厂联合生成氨气、尿素[CO(NH2)2]、纯碱的部分工艺流程图. 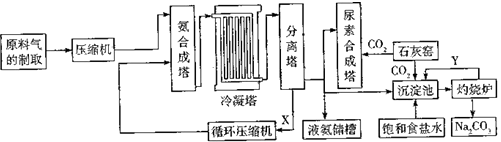
(1)原料气进入压缩机前需要进行净化处理,其目的是 . 制备氨合成塔的材料(填“能”或“不能”)使用普通的碳素钢.
(2)N2、H2混合气体经压缩后再送入氨合成塔,优点是 . 某整个生产中循环使用某些原料可提高生产效益,能循环利用的物质是 .
(3)请按要求填写下列空白.
①沉淀池中的离子方程式: .
②生产尿素的化学方程式: .
(4)在较低温度下,可从沉淀池的溶液中分离出一种副产品由此可推断,低温下NH4C1的溶解度很可能(填“小于”或“大于”)NaCL.NH4C1是一种氮肥,但长期施用易使土壤酸化,用离子方程式表示其原因 .
(5)以焦炭、水为原料制备H2 (碳转化为CO2 , 则1000g纯度为a%((杂质不与水反应)焦炭最多可制备g尿素(已知合成氨时h2的利用率为b%、合成尿素时NH3的利用率为c%)
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种可再生的绿色能源,CO2是一种温室气体,它们都是重要的化工原料.
(1)已知CO的燃烧热△H为﹣283kJmol﹣1 , CO (g)+2H2 (g)CH3OH (1);△H=﹣129kJmol﹣1 , 欲求出CH3OH的燃烧热,则需要知道一个反应,该反应的热化学方程式为 . (反应热直接用△H表示).
(2)向温度不同容积均为1L的a、b、c、d、e五个恒容密闭容器中各充入3molCO2、7molH2O的混合气体,控制适当条件使其同时发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=QkJmol﹣1 , 反应过程中维持各容器温度不变,测得t1时刻各容器中H2O的体积分数(H2O) 如图所示. 
①Q(填“>”或“<”),五个容器中肯定处于非平衡状态的是
②t1时刻时,容器a中正反应速率(填“大于”“小于”或“等于”)容器e中正反应速率.
③Td℃时,该反应的平衡尝试K= .
④欲提高H2的转化率,可采取的措施有(写出两种).
(3)碳捕捉技术的应用既可降低碳排放也可得到重要的化工产品.
①NaOH溶液是常用的碳捕捉剂,若某次捕捉后得到的溶液中c(HCO3﹣):c(CO32﹣)=2:1,则所得溶液的pH=[常温下 K1(H2CO3)=4.4×10﹣7、K2 (HCO3﹣)=5x 1O﹣11].
②在清除锅炉水垢的过程中,需要用Na2CO3将水垢中的CaSO4转化为CaCO3 , 将微溶的CaSO4难溶性的CaCO3的理由是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室里通常用MnO2与浓盐酸反应制取氯气,为进行有关氯气的性质实验,需要4瓶容积为100mL的氯气.(常温下,氯气的密度为2.91g/L)
(1)写出制取氯气的离子方程式.
(2)制取4瓶氯气,理论上需要MnO2固体的质量是多少?
(3)制取4瓶氯气,被氧化的HCl的物质的量是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com