
科目: 来源: 题型:
【题目】CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分.
(1)Cu2+基态的电子排布式可表示为;
(2)SO42﹣的空间构型为(用文字描述);中心原子采用的轨道杂化方式是;写出一种与SO42﹣互为等电子体的分子的化学式:;
(3)向CuSO4 溶液中加入过量NaOH溶液可生成[Cu (OH)4]2﹣ . 不考虑空间构型,[Cu(OH)4]2﹣的结构可用示意图表示为;
(4)资料显示ZnS为难溶物,在活化过程中,CuSO4能转化为CuS的原因是 .
(5)CuS比CuO的熔点(填高或低),原因是 .
(6)闪锌矿的主要成分ZnS,晶体结构如图所示,其晶胞边长为540.0pm,密度为(列式并计算),a位置S2﹣离子与b位置Zn2+离化学﹣选修5:有机化学基础子之间的距离为pm(列式表示). 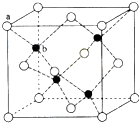
查看答案和解析>>
科目: 来源: 题型:
【题目】下面列出了几组物质,请选择合适物质的序号填在空格上. 同位素;同系物;同分异构体 .
①金刚石和石墨 ②CH3CH2CH2CH3和(CH3)2CHCH3
③ ![]() He和
He和 ![]() He ④CH3CH3 和CH3CH2CH2CH3
He ④CH3CH3 和CH3CH2CH2CH3
⑤ 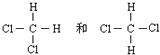 ⑥CH2=CHCH3和CH2=CH2;
⑥CH2=CHCH3和CH2=CH2;
⑦D与T ⑧甲酸乙酯和乙酸甲酯.
查看答案和解析>>
科目: 来源: 题型:
【题目】甲乙丙丁戊是中学常见的无机物,他们的转化关系如图所示(某些条件和部分产物已略去).下列说法错误的是( ) 
A.若戊为一种强碱且焰色反应为黄色,则上述反应可能都属于氧化还原反应
B.常温下,若丙为无色气体,戊为红棕色气体,则甲、乙一定是铜和稀硝酸
C.若甲为硫磺燃烧产物,丁为水,则戊可用于干燥甲
D.若甲为浓盐酸,乙为MnO2 , 则戊可能使品红褪色
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铜矿的主要成分是CuFeS2(硫元素﹣2价,铁元素+2价).实验室用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如图: 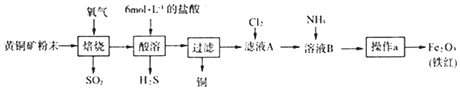
已知:CuFeS2+O2 ![]() Cu+FeS+SO2 FeS+2HCl=FeCl2+H2S↑
Cu+FeS+SO2 FeS+2HCl=FeCl2+H2S↑
(1)实验室制氯气的化学方程式为 .
(2)SO2和H2S有毒,会造成大气污染.
①已知SO2和H2S混合可以得到单质硫.为使SO2和H2S恰好完全转化为硫,二者体积(标准状况)比应为 .
为检验某尾气中是否含有SO2、CO2、CO三种气体,实验小组同学用如下装置设计实验.
选择上述装置(可以重复),按照气流方向其连接顺序为A→(填序号).
(3)PbO2具有强氧化性,可与浓盐酸反应制取氯气.
①上述反应化学方程式为;由PbO与次氯酸钠溶液反应可制得PbO2 , 反应的离子方程式为 .
②Cl2是纺织工业中常用的漂白剂,Na2S2O3可作漂白布匹后的“脱氯剂”.Na2S2O3在溶液中被Cl2氧化成SO42﹣ , 则该反应的化学方程式为 .
③本实验存在的一个缺陷是 .
(4)按上述流程用150g黄铜矿粉末可制得48gFe2O3(铁红),则该黄铜矿中含CuFeS2的质量分数是(假设各步反应均完全进行且过程中无额外物质损耗).
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列问题. I.已知甲和乙为中学常见金属单质,丙和丁为常见气体单质,A~E为常见化合物;A为淡黄色固体,常温下B为液体,C的焰色反应为黄色.试回答下列问题:
(1)A和 E的化学式分别为、;
(2)A+B→C+丙的化学方程式:;
(3)D+C→B+E的离子方程式:;
(4)1mol甲和1mol乙混合投入足量的B中,在标准状况下最多能产生L丁气体.
(5)II.在标准状况下,取甲、乙、丙各30.mL相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝混合物,得下表中有关数据(反应前后溶液体积不发生变化).
实验序号 | 甲 | 乙 | 丙 |
混合物质量/mg | 255 | 385 | 459 |
气体体积/mL | 280 | 336 | 336 |
①甲组实验中,盐酸(填“过量”“适量”或“不足”);乙组实验中,盐酸(填“过量”“适量”或“不足”)
②盐酸的物质的量浓度为mol/L..
③混合物中Mg和Al的物质的量之比为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列问题 I.某校同学为探究Br2、I2和Fe3+的氧化性强弱,进行了如下实验:
①取少量KI溶液于试管中,先加入溴水、振荡,再加入CCl4 , 振荡后静置,观察到下层液体呈紫红色;
②:取少量FeSO4溶液于试管中,先加入溴水,振荡,再继续滴加两滴KSCN溶液,振荡,观察到溶液呈血红色.
(1)写出实验②中发生氧化还原反应的离子方程式: .
(2)由上述两个实验,对物质的氧化性可以得出的正确结论是 .
A.Br2>I2
B.Fe3+>Br2
C.Br2>Fe3+
D.I﹣>Br﹣
(3)II.被誉为“江南小三峡”的南京胭脂河是明代初年开凿的一条人工运河.因其“石有胭脂色”而得名.胭脂河沿岸的那些红色石块的成分是什么?某研究性学习小组取一小块这种红色石块A,粉碎后对其成分进行实验探究,实验记录如图所示. 
请你根据使用推断:
A中含有的酸根离子(填离子符号).B中肯定含有的溶质是(写化学式).
写出实验中有关反应的化学方程式:
②
⑤ .
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计如图装置,研究非金属元素性质变化规律. 
(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色.在化学反应中,强酸一般能制取弱酸.现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择所给试剂,用如上图装置来证明酸性:HNO3>H2CO3>H2SiO3 . (不考虑硝酸的挥发性)A、B、C中盛有的试剂分别为、、 . C中实验现象为;
写出C中发生反应的离子方程式: .
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用上图装置证明氯气氧化性强于碘单质的氧化性.A中盛装浓盐酸,B中装入高锰酸钾粉末,实验时C中溶液变成蓝色,则:C中盛装的试剂为;写出C中离子方程式 . 该实验装置有明显不足,请指出改进方法: .
(3)如果C中盛装饱和的氢硫酸(H2S饱和水溶液),A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀,写出该反应的化学方程式:;如果将SO2气体通入到饱和氢硫酸溶液中,也会产生淡黄色沉淀,该过程体现SO2(填序号). A.漂白性 B.氧化性 C.还原性 D.酸性.
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题: 一定温度下,在一恒容的密闭容器中,由CO和H2合成甲醇:
CO(g)+2H2(g)CH3OH(g)
①下列情形不能说明该反应已达到平衡状态的是(填序号).
A.每消耗1mol CO的同时生成2molH2B.混合气体总物质的量不变
C.CH3OH、CO、H2的浓度都不再发生变化D.生成CH3OH的速率与消耗CO的速率相等
②CO的平衡转化率(α)与温度、压强的关系如图所示.A、B两点的平衡常数K(A)K(B)(填“>”、“=”或“<”).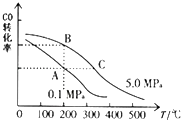
③某温度下,将2.0mol CO和6.0molH2充入2L的密闭容器中,达到平衡时测得c(CO)=0.25mol/L,CO的转化率= , 此温度下的平衡常数K=(保留两位有效数字).
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3 , 含Fe2O3杂质)为原料冶炼铝的工艺流程如下,下列叙述正确的是( ) 
A.试剂X可以是氢氧化钠溶液,也可以是盐酸
B.反应①、过滤后所得沉淀为氢氧化铁
C.图中所示转化反应都不是氧化还原反应
D.反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
查看答案和解析>>
科目: 来源: 题型:
【题目】利用处理废弃的线路板得到含70%Cu、25%Al、4%Fe及少量Au、Pt的金属混合物制备硫酸铜和硫酸铝晶体,流程如图1: 
(1)步骤①~③中过滤操作所需要的玻璃仪器除烧杯、漏斗外还有 .
(2)步骤①中Cu发生的离子方程式为 , 此时该溶液中所有的金属阳离子是;步骤②中得到滤渣2的主要成分是(填化学式).
(3)滤渣3加适量稀硫酸溶解,将得到溶液进行:蒸发浓缩, , 过滤、洗涤,即得到硫酸铜晶体;由滤液3制备Al2(SO4)318H2O时,按化学反应顺序用到的试剂依次为 . (填序号)
①NaOH溶液 ②稀硫酸 ③氨水 ④二氧化碳
(4)在步骤(3)中,发生反应的第一个离子方程式是
(5)为测定制得硫酸铜晶体(CuSO4xH2O)中结晶水含量,取12.5g硫酸铜晶体进行加热分解,得到固体质量与温度的关系如图2.
已知加热过程中,硫酸铜晶体分步失去结晶水.根据图中数据,计算CuSO4xH2O中x的值为;258℃到650℃时反应的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com