
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:阅读理解
 (2012?深圳二模)NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
(2012?深圳二模)NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.| 所加试剂 | 预期现象和结论 |
| 试管A中加足量① 1.0mol/LK淀 粉溶液 1.0mol/LK淀 ;粉溶液 试管B中加1%品红溶液; 试管C中加② 澄清石灰水 澄清石灰水 . |
若A中溶液变蓝色,B中溶液不退色,C中溶液变浑浊.则消毒液部分变质; ③ 若A中溶液变蓝色,B中溶液不退色 (无变化),C中溶液不变浑浊(无变化),则 消毒液未变质 若A中溶液变蓝色,B中溶液不退色 则消毒液未变质;(无变化),C中溶液不变浑浊(无变化),则 消毒液未变质 ④ 若A中溶液不变蓝色(无变化),B中溶 液不退色(无变化),C中溶液变浑浊则消 毒液完全变质 若A中溶液不变蓝色(无变化),B中溶 则消毒液完全变质.液不退色(无变化),C中溶液变浑浊则消 毒液完全变质 |
| (2ab-5vc) |
| 50 |
| (2ab-5vc) |
| 50 |
查看答案和解析>>
科目: 来源: 题型:

| 物质 | 沸点/°C | 在水中 | 在乙醚中 |
| TiCl4 | 136 | 强烈水解 | 易溶 |
| SiCl4 | 58 | 强烈水解 | 易溶 |
| FeCl3 | 303(升华) | 水解 | 易溶 |
| ||
| ||
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
 -C2H5)可生产塑料单体苯乙烯(
-C2H5)可生产塑料单体苯乙烯( -CH=CH2),其原理反应是:
-CH=CH2),其原理反应是: -C2H5(g)
-C2H5(g) 
 -CH=CH2(g)+H2(g);△H=+125kJ?mol-1.某温度下,将0.40mol
-CH=CH2(g)+H2(g);△H=+125kJ?mol-1.某温度下,将0.40mol  -C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
-C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表: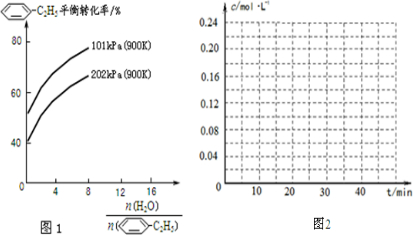
| 时间/min | 0 | 10 | 20 | 30 | 40 |
n( -C2H5)/mol -C2H5)/mol |
0.40 | 0.30 | 0.26 | n2 | n3 |
n( -CH=CH2)/mol -CH=CH2)/mol |
0.00 | 0.10 | n1 | 0.16 | 0.16 |
 -C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将
-C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将 -CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下
-CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下  -C2H5(g)和
-C2H5(g)和 -CH=CH2(g)的浓度c随时间t变化的曲线
-CH=CH2(g)的浓度c随时间t变化的曲线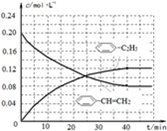

查看答案和解析>>
科目: 来源: 题型:
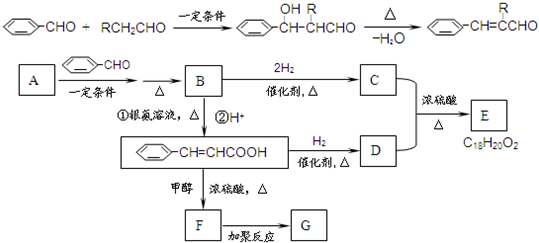
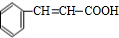 +CH3OH
+CH3OH| 浓硫酸 |
| △ |
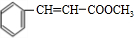 +H2O
+H2O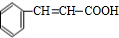 +CH3OH
+CH3OH| 浓硫酸 |
| △ |
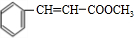 +H2O
+H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com