
科目: 来源: 题型:
【题目】工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为:2FeSO4![]() Fe2O3+ SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验:
Fe2O3+ SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验:
(1)取少量分解得到的固体加入稀盐酸溶解,为检验溶液中是否有Fe3+,下列试剂或药品中最合适的是 (填序号),加入该试剂后可观察的现象为 。
A.稀盐酸 B.氯气 C.KSCN溶液 D.氯化铜溶液
(2)将高温分解产生的气体通入下图所示装置中,以检验产生的气体成分。
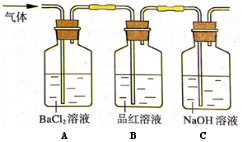
请回答下列问题:
①若在装置A中,观察到有白色沉淀生成,则该沉淀为 ,表明有 气体存在。
②装置C中的NaOH溶液的作用是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】500℃,在三个相同体积的恒容密闭容器里,分别加入对应物质,甲:2mol SO2 1mol O2乙:2mol SO2 1mol O2 1mol N2 丙:4mol SO2 2mol O2同时进行反应,开始时反应速率最大的是( )
A.甲
B.乙
C.丙
D.无法判断
查看答案和解析>>
科目: 来源: 题型:
【题目】氮的化合物在生产生活中广泛存在.
(1)处理生活污水中的NH4+ , 过程如图1: 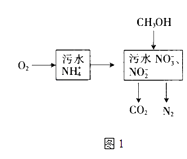
①根据较新的研究表明,将只含NO2﹣的污水与含NH4+的污水按比例混合,直接转化为无毒气体,该气体为 .
②空气将NH4+转变为NO3﹣或NO2﹣ , 溶液pH(填“增大”、“减小”或“不变”).
③完全处理含1mol NH4+污水,则n(O2)与n(CH3OH)关系式为[用n(O2)与n(CH3OH)表示].
(2)用焦炭还原NO2的反应为:2NO2(g)+2C(s )N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图2所示: 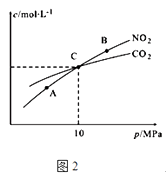
①A、B两点的浓度平衡常数关系:Kc(A)Kc(B) (填“>”、“<”或“﹦”).
②A、B、C三点中NO2的转化率最高的是(填“A”或“B”或“C”)点.
③计算C点时该反应的压强平衡常数Kp(C)=(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下甲醇与一氧化碳反应可以合成乙酸.通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO﹣),用含a和b.的代数式表示该混合溶液中醋酸的电离常数为: .
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,向一定体积0.1molL﹣1的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液pOH[pOH=﹣lgc(OH﹣)]与pH的变化关系如图所示,则( ) 
A.N点处pH>pOH,则N点处所示溶液呈酸性
B.该温度下水的离子积Kw=1×10﹣2a
C.Q点所示溶液呈中性,则M,N,Q三点中只有Q点溶液中水的电离出的c(H+)与水的电离c(OH﹣)相等
D.M点所示溶液的导电能力强于Q
查看答案和解析>>
科目: 来源: 题型:
【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:请回答: 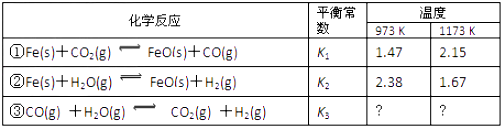
三个反应的平衡常数分别为K1、K2和K3推断反应③为△H30(填“>”成“<”)根据反应①和反应②可推导出K1、K2和K3的关系式:
查看答案和解析>>
科目: 来源: 题型:
【题目】在200 mL由NaCl、MgCl2、KCl组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
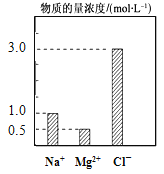
(1)该混合液中,NaCl的物质的量的浓度为 molL-1,含溶质MgCl2的物质的量为 mol。
(2)该混合液中KCl的质量为 g。
查看答案和解析>>
科目: 来源: 题型:
【题目】将铁粉、铜粉、FeCl3溶液和CuCl2溶液混合于某容器中充分反应(假定容器不参与反应)。试判断下列情况下,容器中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器中不可能有的离子是________,铜单质______(填“一定”或“可能”)存在。
(2)若CuCl2有剩余,则容器中还可能有的离子为________,铜单质______(填“一定”或“可能”)存在。
(3)若FeCl3和CuCl2都有剩余,则容器中不可能有的单质是______,Fe2+_____(填“一定”或“可能”)存在。
(4)将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL 0.5mol/LFeSO4溶液和5.2g固体沉淀物,则原Fe2(SO4)3和CuSO4的混合溶液中Fe2(SO4)3的物质的量浓度为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)CO(g)+3H2(g)设起始 ![]() =Z,在恒压下,平衡时CH4的体积分数φ(CH4)与Z和T(温度)的关系如图所示,下列说法错误的是( )
=Z,在恒压下,平衡时CH4的体积分数φ(CH4)与Z和T(温度)的关系如图所示,下列说法错误的是( ) 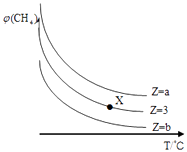
A.该反应的焓变△H>0
B.图中Z的大小为b>3>a
C.图中X点对应的平衡混合物中 ![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后φ(CH4)增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com