
科目: 来源: 题型:

| 10-12 |
| a3bd2 |
| 10-12 |
| a3bd2 |
查看答案和解析>>
科目: 来源: 题型:
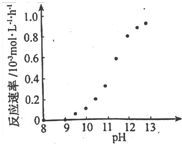 (2012?福建)(1)电镀时,镀件与电源的
(2012?福建)(1)电镀时,镀件与电源的查看答案和解析>>
科目: 来源: 题型:



| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
查看答案和解析>>
科目: 来源: 题型:阅读理解
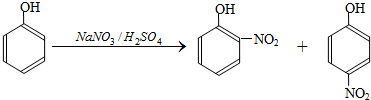
| 密度 (g?mL-1) |
熔点 (℃) |
沸点 (℃) |
溶解性 | 其他 | |
| 邻硝基苯酚 | 1.495 | 44.45 | 214 | 微溶于冷水,易溶于热水 | 能与水蒸气一同挥发 |
| 对硝基苯酚 | 11.481 | 113.4 | 279 | 稍溶于水 | 不与水蒸气一同挥发 |
查看答案和解析>>
科目: 来源: 题型:
 (2011?南京三模)核能源已日益成为当今世界的主要能源.
(2011?南京三模)核能源已日益成为当今世界的主要能源.查看答案和解析>>
科目: 来源: 题型:阅读理解
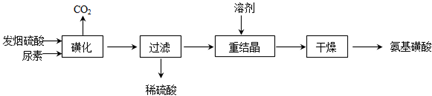
查看答案和解析>>
科目: 来源: 题型:
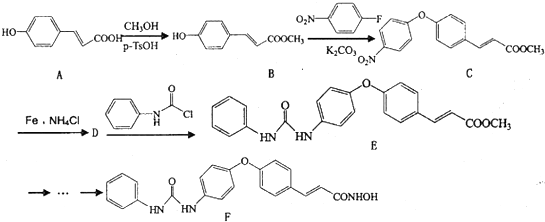







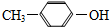 ,)和乙炔为主要原料制备化合物A的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
,)和乙炔为主要原料制备化合物A的合成路线流程图(无机试剂任选).合成路线流程图示例如下:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com