
科目: 来源: 题型:阅读理解
| 气体 | SO2 | N2 | O2 |
| 物质的量 | 10 | 58 | 6 |
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量(g) | 2.812 | 5.624 | 8.436 |
| 生成气体的体积(L)(标准状况) | 1.120 | 2.240 | 2.800 |
查看答案和解析>>
科目: 来源: 题型:

| H+ |


 的化学方程式:
的化学方程式:



查看答案和解析>>
科目: 来源: 题型:
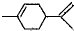 .
.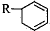 (R代表烃基),写出A可能的两种结构简式
(R代表烃基),写出A可能的两种结构简式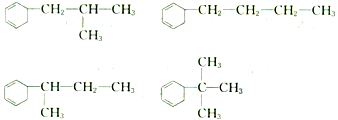 (四种中的任意两种)
(四种中的任意两种) (四种中的任意两种)
(四种中的任意两种)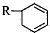 表示)和Cl2发生1,4-加成反应的化学方程式:
表示)和Cl2发生1,4-加成反应的化学方程式: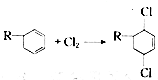

查看答案和解析>>
科目: 来源: 题型:阅读理解
| 实验编号 | 1 | 2 | 3 |
| 消耗Na2S2O3体积/mL | 26.90 | 27.00 | 26.96 |
查看答案和解析>>
科目: 来源: 题型:阅读理解

| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
 (2012?闵行区二模)研究和开发CO2和CO的创新利用是环境保护和资源利用的双赢课题.CO可用于合成甲醇.在压强为0.1MPa条件下,在体积为b L的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:CO(g)+2H2(g)?CH3OH(g),平衡时CO的转化率与温度、压强的关系如图:
(2012?闵行区二模)研究和开发CO2和CO的创新利用是环境保护和资源利用的双赢课题.CO可用于合成甲醇.在压强为0.1MPa条件下,在体积为b L的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:CO(g)+2H2(g)?CH3OH(g),平衡时CO的转化率与温度、压强的关系如图:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:



| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com