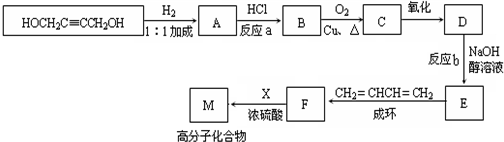
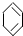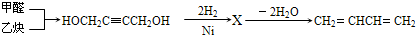(2009?松江区二模)复印机使用的墨粉主要成份是Fe
3O
4,如图是氧化沉淀法生产Fe
3O
4的工艺:

已知:①工业绿矾中FeSO
4的含量为52.5%,其中的杂质不参与反应;
②Fe(OH)
2+2Fe(OH)
3→Fe
3O
4?4H
2O
请回答下列问题:
(1)铁的常见氧化物有
FeO、Fe2O3、Fe3O4
FeO、Fe2O3、Fe3O4
;
(2)Fe
3O
4与盐酸反应的化学方程式是:
Fe3O4+8HCl→FeCl2+2FeCl3+4H2O
Fe3O4+8HCl→FeCl2+2FeCl3+4H2O
,检验反应后的溶液中含Fe
3+的方法:
取待测液少许于试管中,加入适量的KSCN溶液,若溶液显血红色,则证明含Fe3+
取待测液少许于试管中,加入适量的KSCN溶液,若溶液显血红色,则证明含Fe3+
;
(3)在工艺流程中,通入适量空气“氧化”时的化学方程式是:
4Fe(OH)2+2H2O+O2→4Fe(OH)3
4Fe(OH)2+2H2O+O2→4Fe(OH)3
;
(4)生产中可获得的副产品是
Na2SO4?10H2O
Na2SO4?10H2O
,提取该副产品的操作顺序是:
bcdae
bcdae
(填写序号)
a.过滤 b.加热浓缩 c.冷却 d.结晶 e.洗涤
(5)在生产过程中,若工业绿矾的投料速率是12.16kg/h,为使产品较纯,鼓入空气的速率应为
0.784
0.784
m
3/h(假设反应在标准状态下进行,空气中O
2占20%).

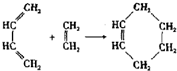 (也可表示为:
(也可表示为: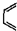 +║→
+║→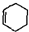 )
)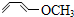 b.
b.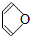 c.
c. d.
d.