
科目: 来源: 题型:
【题目】某有机物的结构如下图所示,下列说法正确的是

A. 分子式为C10H14O3 B. 可发生加成、取代、氧化、加聚等反应
C. 与足量溴水反应后官能团数目不变 D. 1mol该有机物可与2molNaOH反应
查看答案和解析>>
科目: 来源: 题型:
【题目】向10 mL0.1 mol·L-1NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL。下列叙述正确的是
A. x=10时, 溶液中有NH4+、AlO2-、SO42-, 且c(NH4+)>c(SO42-)
B. x=10时, 溶液中有NH4+、Al3+、SO42-, 且c(NH4+)>c(Al3+)
C. x=30时, 溶液中有Ba2+、AlO2-、OH-, 且c(OH-)<c(AlO2-)
D. x=30时, 溶液中有Ba2+、Al3+、OH-, 且c(OH-)=c(Ba2+)
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
A. 0.1 mol 的![]() 中,含有
中,含有![]() 个中子
个中子
B. pH=1的H3PO4溶液中,含有![]() 个
个![]()
C. 2.24L(标准状况)苯在O2中完全燃烧,得到![]() 个CO2分子
个CO2分子
D. 密闭容器中1 mol PCl3与1 mol Cl2反应制备 PCl5(g),增加![]() 个P-Cl键
个P-Cl键
查看答案和解析>>
科目: 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列说法正确的是( )
A. 常温常压下,64g SO2中含有的原子数为3NA
B. 标准状况下,11.2L CCl4所含原子数目为2.5NA
C. 2L 0.1 molL﹣1K2SO4溶液中含K+物质的量为0.2 mol
D. 1.0 mol CH4与Cl2在光照下反应生成的CH3Cl分子数为1.0NA
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某反应A(g)+B(g)=C(g)+D(g),过程中的能量变化如图所示,下列说法中正确的是( )
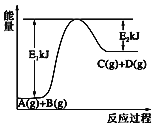
A. A的能量一定低于C
B. 反应物断键吸收的总能量大于产物新键形成放出的总能量
C. 化学反应中的能量变化都表现为热量的变化
D. 1mol气体A和1mol气体B反应生成1mol气体C和1molD
查看答案和解析>>
科目: 来源: 题型:
【题目】某探究小组用盐酸与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HCl浓度为1.00mol/L、2.50mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、40℃,每次实验盐酸的用量为25.00mL,大理石用量为10.00g。
(1)写出盐酸与大理石反应的化学方程式________
(2)请完成以下实验设计表,并把实验中空缺处补充完整:
实验 编号 | 温度 (℃) | 大理石 规格 | HCl浓度(mol/L) | 实验目的 |
① | 25 | 粗颗粒 | 2.50 | (I)实验①和②探究温度对反应速率的影响; (II)实验①和③探究浓度对反应速率的影响; (III)实验①和④探究______对反应速率的影响 |
② | __ | 粗颗粒 | 2.50 | |
③ | 25 | 粗颗粒 | ___ | |
④ | 25 | 细颗粒 | 2.50 |
(3)实验①中CO2质量随时间变化的关系见下图。计算实验①中70s-90s范围内用HCl表示的平均反应速率 ______(忽略溶液体积变化)

查看答案和解析>>
科目: 来源: 题型:
【题目】只用一种试剂可鉴别K2SO4、MgCl2、FeCl2、(NH4)2SO4四种溶液,这种试剂是
A. Ba(OH)2 B. H2SO4 C. NaOH D. AgNO3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子,能大量共存的是
A. NH4+、Ba2+、Cl-、OH- B. Na+、K+、CO32-、SO32-
C. Na+、Mg2+、OH-、HCO3- D. K+、Fe3+、SO42-、I-
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)已知2H→H2放出437.6 kJ的热量,下列说法正确的是____
A.氢气分子内每个氢原子都达到稳定结构
B.氢气分子的能量比两个氢原子的能量低
C.1molH2离解成 2 mol H 要放出437.6 kJ热量
D.氢原子比氢气分子稳定
(2)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O![]() 2H2↑+O2↑。制得的氢气可用于制作燃料电池.试回答下列问题:
2H2↑+O2↑。制得的氢气可用于制作燃料电池.试回答下列问题:
①分解海水时,实现了光能转化为__能;生成的氢气用于制作燃料电池时,实现了化学能转化为____能;分解海水的反应属于___反应(填“放热”或“吸热”)
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为:2H2+2O24e=2H2O,则B极的电极反应式为:____
(3)已知某电池的总反应为:Zn+2MnO2+2NH4Cl=ZnCl2+2NH3↑+Mn2O3+H2O,写出该电池的电极反应方程式:负极_______正极_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com