
科目: 来源: 题型:
【题目】“绿色化学”实验已走进课堂,下列做法符合“绿色化学”的是

①实验室收集氨气采用图甲所示装置
②实验室中做氯气与钠的反应实验时采用图乙所示装置
③实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验
④实验室中采用图丙所示装置进行铜与稀硝酸的反应
A. ②③④
B. ①②③
C. ①②④
D. ①③④
查看答案和解析>>
科目: 来源: 题型:
【题目】假定把12C的相对原子质量定为24,把24g12C含有的原子个数定为阿伏加德罗常数,而物质的量的概念不变。则下列推断不正确的是
A. 此时16O的相对原子质量为32
B. 40gNaOH溶于水配成1L溶液,其物质的量浓度为1 mol/L
C. 标况下44gCO2的体积为22.4L
D. NA个氧分子与NA个氢分子有相同数目的分子
查看答案和解析>>
科目: 来源: 题型:
【题目】关于下列各实验装置的叙述中,不正确的是

A. 装置①可用于实验室制取少量NH3或O2
B. 可用从a处加水的方法检验装置②的气密性
C. 实验室不可用装置③收集HCl
D. 验证溴乙烷发生消去反应生成烯烃的实验可利用装置④进行
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期的三种元素X、Y、Z,已知X元素的原子最外只有一个电子,Y元素的原子M层上的电子数是它K层和L层电子总数的一半,Z元素原子的L层上的电子数比Y元素原子的L层上的电子数少2个,则这三种元素所组成的化合物的化学式不可能的是( )
A. X3YZ4 B. X3YZ3 C. X2YZ4 D. X4Y2Z7
查看答案和解析>>
科目: 来源: 题型:
【题目】钠硝石又名智利硝石,主要成分为NaNO3。据最新勘探预测表明,我国吐鲁番盆地钠硝石资源量约2.2亿吨,超过了原世界排名第一的智利。一种以钠硝石为原料制备KNO3的流程如下图所示(矿石中其他物质均忽略):

相关化合物溶解度随温度变化曲线如下图所示:

回答下列问题:
(1) NaNO3是________________(填“电解质”或“非电解质”)。
(2) 一定温度下,NaNO3可分解生成Na2O、NO和O2,该反应的化学方程式为__________________。
(3) 为提高钠硝石的溶浸速率,可对矿石进行何种预处理________________(答出一种即可)。
(4) 为减少KNO3的损失,步骤a的操作应为:________________________________;
步骤b中控制温度可为下列选项中的________。
A.10℃ B.40℃ C.60℃ D.90℃
(5) 如何验证洗涤后的KNO3中没有Cl-:_______________________________________。
(6) 若100吨钠硝石可生产60.6吨KNO3,则KNO3的产率为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某装有红色溶液的试管,加热时溶液颜色逐渐变浅,则原溶液可能是
①滴有酚酞的氨水溶液 ②滴有酚酞的氢氧化钠溶液
③溶有SO2的品红溶液 ④滴有酚酞的饱和氢氧化钙溶液
⑤酚酞溶液中滴加少量NaClO溶液
A. ①④⑤ B. ①③ C. ③④⑤ D. ①④
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钾(K2FeO4)为紫黑色粉末,是一种新型高效消毒剂。K2FeO4易溶于水,微溶于浓KOH溶液,在0 ℃~5 ℃的强碱性溶液中较稳定。一般制备方法是先用Cl2与KOH溶液在20 ℃以下反应生成KClO(在较高温度下则生成KClO3),KClO再与KOH、Fe(NO3)3溶液反应即可制得K2FeO4。实验装置如图所示:
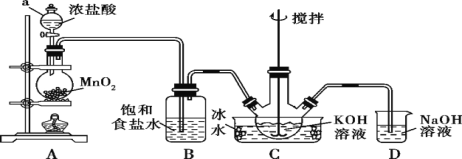
回答下列问题:
(1)制备KClO。
①仪器a的名称是________________;装置B吸收的气体是________。
②装置C中三颈烧瓶置于冰水浴中的目的是______________;装置D的作用是_____________。
(2)制备K2FeO4。
①装置C中得到足量KClO后,将三颈烧瓶上的导管取下,加入KOH溶液、Fe(NO3)3溶液,水浴控制反应温度,搅拌,当溶液变为紫红色,该反应的离子方程式为________________________________。
②向装置C中加入饱和________溶液,析出紫黑色晶体,过滤。
(3)测定K2FeO4纯度。测定K2FeO4的纯度可用滴定法,滴定时有关反应的离子方程式为:
a.FeO42-+CrO2-+2H2O═CrO42-+Fe(OH)3↓+OH-
b.2CrO42-+2H+═Cr2O72-+H2O
c.Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
称取2.0g制备的K2FeO4样品溶于适量KOH溶液中,加入足量的KCrO2,充分反应后过滤,滤液在250mL容量瓶中定容.取25.00mL加入稀硫酸酸化,用0.10 molL-1的(NH4)2Fe(SO4)2标准溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液的体积为24.00mL,则该K2FeO4样品的纯度为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com