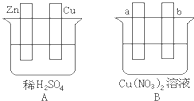
Ⅰ.用导线将A、B两装置的四个电极进行连接,使a极析出铜.回答有关问题.
(1)导线将容器A和B连接时,Zn接
a
a
,Cu接
b
b
(填“a”或“b”)
(2)容器A中Cu极发生的电极反应为
2H++2e-=H2↑
2H++2e-=H2↑
.
(3)B装置叫
电解池
电解池
,溶液中的NO
3-向
b
b
极移动(填“a”或“b”).
(4)若b极观察到有无色无味气泡产生,经过一段时间后,停止反应并搅拌均匀,溶液的pH值将
降低
降低
(填“升高”、“降低”或“不变”),加入一定量的
CuO
CuO
后(填化学式),溶液能恢复至与反应前完全一致.若反应一段时间后,测得溶液中Cu
2+浓度没有明显下降,可能的原因是:
B装置是电镀池
B装置是电镀池
.
Ⅱ.炒菜的铁锅没有洗干净容易生锈.用必要的文字和有关化学方程式说明铁锈是如何形成的
铁、碳和氯化钠溶液构成原电池,铁作负极而被腐蚀,碳作正极,正极上氧气得电子生成氢氧根离子,氢氧根离子和亚铁离子反应生成氢氧化亚铁,氢氧化亚铁不稳定易被氧化生成氢氧化铁,氢氧化铁失水生成铁锈,反应方程式为:2Fe+O2+2H2O=2Fe(OH)2,4Fe(OH)2+2H2O+O2=4Fe(OH)3
铁、碳和氯化钠溶液构成原电池,铁作负极而被腐蚀,碳作正极,正极上氧气得电子生成氢氧根离子,氢氧根离子和亚铁离子反应生成氢氧化亚铁,氢氧化亚铁不稳定易被氧化生成氢氧化铁,氢氧化铁失水生成铁锈,反应方程式为:2Fe+O2+2H2O=2Fe(OH)2,4Fe(OH)2+2H2O+O2=4Fe(OH)3
.

 Ⅰ.用导线将A、B两装置的四个电极进行连接,使a极析出铜.回答有关问题.
Ⅰ.用导线将A、B两装置的四个电极进行连接,使a极析出铜.回答有关问题.