为测定该补血剂样品[主要成分是硫酸亚铁晶体(FeSO
4?7H
2O)]中铁元素的含量,某化学兴趣小组设计了两套实验方案:
方案一:用酸性KMnO
4溶液滴定测定铁元素的含量
(1)写出滴定反应的离子方程式
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
.
(2)下列滴定方式中,最合理的是
B
B
(夹持部分略去)(填字母序号).

(3)实验前,首先要准确配制一定物质的量浓度的KMnO
4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
250mL容量瓶
250mL容量瓶
(填仪器名称).
(4)某同学设计以原电池的形式实现Fe
2+至Fe
3+的转化,电解质溶液为稀硫酸,请写出负极的电极反应式
Fe2+-e-═Fe3+
Fe2+-e-═Fe3+
方案二 将FeSO
4转化为Fe
2O
3,测定质量变化操作流程如下:

(3)步骤②中除用H
2O
2外还可以使用的物质是
氯水
氯水
.
(5)步骤②是否可以省略
不能
不能
,理由是
Fe2+与碱反应后不能保证Fe2+全部转化为Fe3+,加热不能得到纯净的Fe2O3,故无法准确计算Fe的含量
Fe2+与碱反应后不能保证Fe2+全部转化为Fe3+,加热不能得到纯净的Fe2O3,故无法准确计算Fe的含量
.
(6)步骤④中一系列操作依次是:过滤、洗涤、
灼烧
灼烧
、冷却、称量.
(7)假设实验无损耗,则每片补血剂含铁元素的质量
0.07a
0.07a
g(用含a的代数式表示).




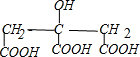
 +H2O
+H2O
 +H2O
+H2O +4NaOH
+4NaOH +CH3COONa+4H2O+4CH3CH2CH2CH2OH
+CH3COONa+4H2O+4CH3CH2CH2CH2OH +4NaOH
+4NaOH +CH3COONa+4H2O+4CH3CH2CH2CH2OH
+CH3COONa+4H2O+4CH3CH2CH2CH2OH 甲、乙、丙、丁是由前20号元素组成的物质,有如下转化:甲+乙→丙+丁
甲、乙、丙、丁是由前20号元素组成的物质,有如下转化:甲+乙→丙+丁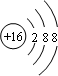

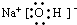
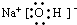
 H++HO2ˉ
H++HO2ˉ H++HO2ˉ
H++HO2ˉ
