
科目: 来源: 题型:
| 实验步骤 | 向3-4mL 1mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全 |
| 实验现象 | 产生白色沉淀 |
| 离子方程式 | (1)Ca2++SO42-=CaSO4↓ (1)Ca2++SO42-=CaSO4↓ |
| 小组讨论交流 | 向上述反应后的清液中滴入适量1mol/L的Na2CO3 溶液会出现什么现象 |
| 假设出现的实验现象,说明理由 | 假设:Ⅰ无现象 理由:反应没有限度,Ca2+沉淀完全 假设:Ⅱ (2)产生白色沉淀 (2)产生白色沉淀 ,理由:反应存在限度,溶液中尚有较多Ca2+ 反应存在限度,溶液中尚有较多Ca2+ |
| 证明你的假设 | 现象:产生大量的白色沉淀 |
| 离子方程式 | (3)Ca2++CO32-=CaCO3↓ (3)Ca2++CO32-=CaCO3↓ |
| 解释 | (4)加入CO32-产生了大量的白色沉淀,说明Ca2++SO42-  CaSO4↓反应是可逆反应,存在反应限度,所以Ca2+不能反应完,才出现这种现象 CaSO4↓反应是可逆反应,存在反应限度,所以Ca2+不能反应完,才出现这种现象(4)加入CO32-产生了大量的白色沉淀,说明Ca2++SO42-  CaSO4↓反应是可逆反应,存在反应限度,所以Ca2+不能反应完,才出现这种现象 CaSO4↓反应是可逆反应,存在反应限度,所以Ca2+不能反应完,才出现这种现象 |
查看答案和解析>>
科目: 来源: 题型:
 →
→
 →
→
 +Ca2++
+Ca2++ →
→
 +Ca2++
+Ca2++ →
→
查看答案和解析>>
科目: 来源: 题型:



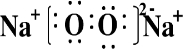
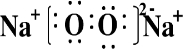
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
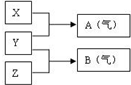 (1)有人将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:
(1)有人将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com