
科目: 来源: 题型:
 如图所示是测定镁粉(含有少量杂质Al)纯度的实验装置,所用NaOH溶液的浓度为4.5mol/L,体积为100mL,不同时间段电子天平的读数如下表所示:
如图所示是测定镁粉(含有少量杂质Al)纯度的实验装置,所用NaOH溶液的浓度为4.5mol/L,体积为100mL,不同时间段电子天平的读数如下表所示:| 实验操作 | 时间(min) | 电子天平的读数(g) |
| 烧杯+NaOH溶液 | 120.0 | |
| 烧杯+NaOH溶液+样品 | 0 | 135.6 |
| 1 | 135.1 | |
| 2 | 134.7 | |
| 3 | 134.4 | |
| 4 | 134.4 |
查看答案和解析>>
科目: 来源: 题型:
| 实验内容 | 主要实验操作 | 主要结论 | |
| ① | 除去FeSO4溶液中的少量Fe2(SO4)3, | 过量铁粉 过量铁粉 ,过滤 |
离子方程式为: |
| ② | 证明SO2既有漂白性又有还原性 | 主要现象为: | |
| ③ | 证明还原性: I->Cl- |
取样, 滴加氯水 滴加氯水 并用四氯化碳萃取 并用四氯化碳萃取 . |
离子方程式为: |
| ④ | 证明CO2具有一定的氧化性(助燃性): | 化学方程式为: |
查看答案和解析>>
科目: 来源: 题型:
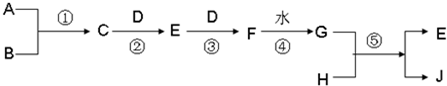
| ||
| 高温高压 |
| ||
| 高温高压 |
查看答案和解析>>
科目: 来源: 题型:
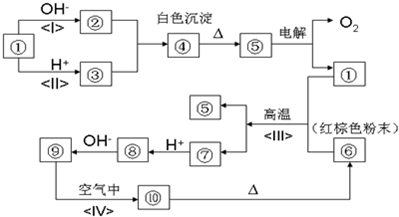
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com