A、B、D、E、Y为5种短周期元素.
①A、B、D位于同一周期,D、Y位于同一主族.A的原子的最外层电子数是其次外层电子数的2倍.
②D的氢化物是最常用的溶剂,E的单质是一种生活中常见的金属.
请回答:
(1)AD
2中具有的化学键的类型是
极性共价键
极性共价键
.
(2)高温时,6g A的单质与D的气态氢化物反应,生成两种还原性气体,吸收的热量为65.75kJ,其反应的热化学方程式是
C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ/mol
C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ/mol
.
(3)D与氢元素可组成含有10个电子的X
-,与X
-组成元素相同,原子数个数比也相同的分子的电子式是
.
(4)将盛有一定量红棕色气体BD
2的4L容器压缩至2L,待气体颜色不再变化时,容器内的压强(填“大于”、“等于”或“小于”)
小于
小于
原来的2倍,原因是
2NO2?N2O4为可逆反应,当将其体积压缩为原来的一半时,平衡向右移动,容器内气体分子总数减少,容器内压强小于原来的2倍
2NO2?N2O4为可逆反应,当将其体积压缩为原来的一半时,平衡向右移动,容器内气体分子总数减少,容器内压强小于原来的2倍
.
(5)E的某种化合物可用作净水时的混凝剂,其原理是(用离子方程式表示)
Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.
(6)YD
2气体通入足量BaCl
2和B的最高价氧化物对应的水化物的混合溶液中,生成白色沉淀和无色气体,反应的离子方程式是
3Ba2++3SO2+2NO3-+2H2O=3BaSO4↓+2NO↑+4H+
3Ba2++3SO2+2NO3-+2H2O=3BaSO4↓+2NO↑+4H+
.

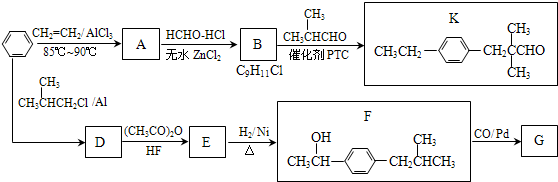
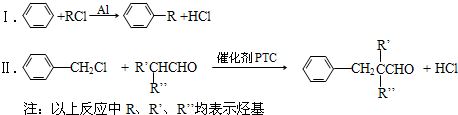
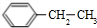

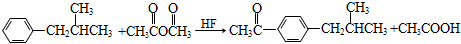
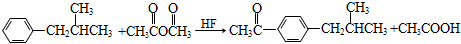
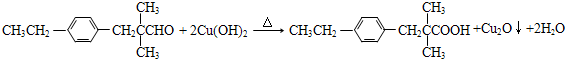
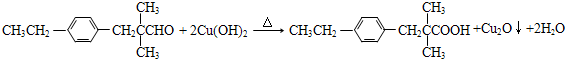

 某同学设计了如图所示装置(部分夹持装置已略去)进行实验研究.请回答:
某同学设计了如图所示装置(部分夹持装置已略去)进行实验研究.请回答:


 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )