
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:阅读理解


| 1 | 2 |
查看答案和解析>>
科目: 来源: 题型:
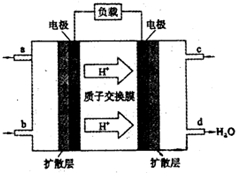 甲醇(CH3OH)燃料电池被认为是很有应用前景的燃料电池.下图是自呼吸式甲醇燃料电池工作示意图.电池总反应:2CH3OH+3O2=2CO2+4H2O,则图中进入c口的物质是( )
甲醇(CH3OH)燃料电池被认为是很有应用前景的燃料电池.下图是自呼吸式甲醇燃料电池工作示意图.电池总反应:2CH3OH+3O2=2CO2+4H2O,则图中进入c口的物质是( )查看答案和解析>>
科目: 来源: 题型:
 某粉末试样由几种常见氧化物组成.向该粉末试样中加入过量的氢氧化钠溶液,充分溶解后过滤得红棕色固体和无色溶液,向所得无色溶液中滴入盐酸,产生沉淀的质量与所加盐酸的体积的关系如图所示,组成该粉末试样的氧化物可能是( )
某粉末试样由几种常见氧化物组成.向该粉末试样中加入过量的氢氧化钠溶液,充分溶解后过滤得红棕色固体和无色溶液,向所得无色溶液中滴入盐酸,产生沉淀的质量与所加盐酸的体积的关系如图所示,组成该粉末试样的氧化物可能是( )查看答案和解析>>
科目: 来源: 题型:
| ||
 或
或
 或
或
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 新修改的《机动车驾驶证申领和使用规定》于2010年4月1日起实施,新规规定酒驾一次扣12分,出此重拳治理酒驾是因为酒后驾车是引发交通事故的重要原因.如图为交警对驾驶员是否饮酒进行检测.其原理如下:
新修改的《机动车驾驶证申领和使用规定》于2010年4月1日起实施,新规规定酒驾一次扣12分,出此重拳治理酒驾是因为酒后驾车是引发交通事故的重要原因.如图为交警对驾驶员是否饮酒进行检测.其原理如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com